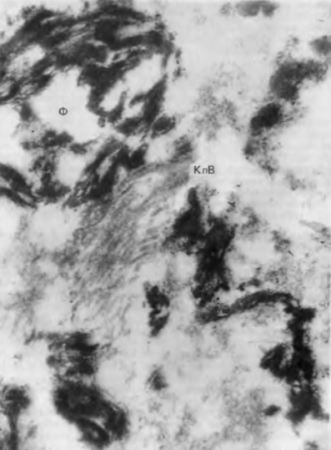
Стромально-сосудистые или мезенхимальные дистрофии развиваются в тканях, производных мезенхимы, в первую очередь в интерстициальной соединительной ткани, составляющей строму органов и стенки сосудов. Она состоит из коллагеновых, эластичных и ретикулиновых волокон, внеклеточного матрикса, представленного гликозаминогликанами; фибробластов, продуцирующих такие белки, как коллаген и эластин: гистиоцитов. В интерстициальной соединительной ткани располагаются кровеносные и лимфатические сосуды микроциркуляторного русла, нервные окончания, рециркулирующие лимфоциты и резидентные макрофаги. В зависимости от вида нарушения обмена веществ стромально-сосудистые дистрофии делят на белковые (диспротеинозы), жировые (липидозы) и углеводные.
БЕЛКОВЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Белковые стромально-сосудистые дистрофии (диспротеинозы) включают следующие виды нарушения белкового обмена: мукоидное набухание, фибриноидное набухание (фибриноид), гиалиноз и амилоидоз.
Мукоидное набухание.
Его причиной могут быть инфекционно-аллергические заболевания, в том числе ревматические болезни, атеросклероз, гипертоническая болезнь и др. Основным механизмом развития является инфильтрация.
Морфология. Дистрофия характеризуется поверхностной и обратимой дезорганизацией соединительной ткани в строме органов и в стенках сосудов за счет накопления и перераспределения гликозаминогликанов, главным образом гиалуроновой кислоты.
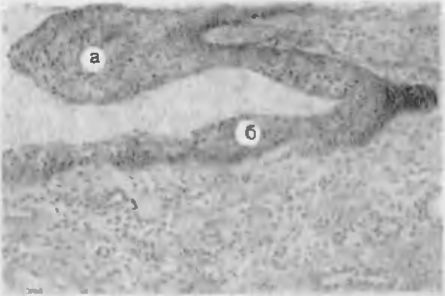
Рис. 5. Мукоидное набухание клапана сердца (ревматический эндокардит). В клапане сердца (а) и париетальном эндокарде (б) — резкая метахромазия Умеренная лимфогистиоцитарная инфильтрация ткани клапана. Окраска толуидиновым синим.
Гликозаминогликаны обладают гидрофильными свойствами, и их накопление в строме органов и в стенках сосудов ведет к повышению сосудистой проницаемости, выходу в ткани мелкодисперсных белков плазмы крови и гликопротеинов. При этом происходит лишь набухание, но не разрушение коллагеновых волокон и внеклеточного матрикса. Однако коллагеновые волокна теряют устойчивость к коллагеназе и приобретают способность при окраске толуидиновым синим изменять голубой цвет на сиреневый (рис. 5). Это явление называется метахромазией и указывает на развитие мукоидного набухания, не имеющего клинической симптоматики. Наиболее хорошо метахромазия выражена в стенках артерий, эндокарде, клапанах сердца, синовиальных оболочках. При этом органы внешне не изменены, функция их снижена незначительно.
Фибриноидное набухание.
Фибриноид является следующей стадией развития стромально-сосудистой дистрофии.
Механизмы фибриноида — декомпозиция и инфильтрация.
Морфология: глубокая и необратимая дезорганизация соедини-i тельной ткани стромы органов и стенок сосудов. Усиливается выход из сосудов плазмы, плазменных белков, причем не только мелкодисперсных, но и таких крупнодисперсных, как фибриноген, который в соединительной ткани превращается в фибрин. Происходит накопление фибрина, гликозаминогликанов и других белков между фазами коллагеновых волокон, во внеклеточном матриксе и в стенках сосудов. В результате этого они вначале резко набухают и возникает фибриноидное набухание, а затем разрушаются. Остатки коллагеновых и эластических волокон вместе с набухшим и резко измененным внеклеточным матриксом превращаются в гомогенную, рыхлую, бесструктурную массу. Развивается фибриноидный некроз (рис. 6).
Функция органов при этом отчетливо страдает, так как при фибриноидном некрозе стенок сосудов в них нарушается кровоток. Например, при фибриноидном некрозе капилляров клубочков почек может развиться острая почечная недостаточность. Заканчивается фибриноид гиалинозом или склерозом.
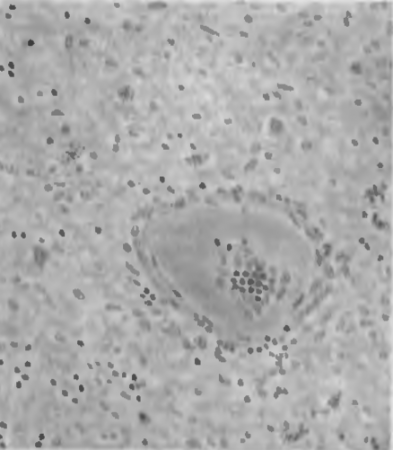
Рис. 7. Гиалиноз артериолы мозга при гипертонической болезни. Стенка артериолы утолщена, состоит из однородного гиалиноподобного вещества, просвет резко сужен. Ткань мозга отечна.
Гиалиноз может быть завершающей стадией дезорганизации соединительной ткани, но может быть и самостоятельным видом стромально-сосудистых дистрофий. Основными механизмами ее развития являются декомпозиция и инфильтрация.
Морфология. Гиалин представляет собой белок, в состав которого входят разрушенные компоненты соединительной ткани, плазменные белки, иммуноглобулины, комплемент, липиды. Внешне этот белок напоминает гиалиновый хрящ, с чем связано название дистрофии.
Гиалинозу артериол и мелких артерий предшествует выраженное повышение сосудистой проницаемости и пропитывание их стенок плазмой, содержащей белки, а при некоторых заболеваниях и липиды (плазморрагия). Это связано либо с повторяющимися спазмами и паралитическими расширениями артериол, чаще при гипертонической болезни, либо с повреждением стенок cocyдов, например, циркулирующими иммунными комплексами (при сахарном диабете). Происходит коагуляция белков, скапливающихся в стенках артериол; стенки становятся гомогенными, утолщенными, хрупкими, теряют эластичность, просветы сосудов уменьшаются, в них снижается кровоток (рис. 7). Такие артериолы, особенно в головном мозге, часто разрываются и происходит
кровоизлияние в мозг. Гиалиноз артериол почечных клубочков приводит к их гибели, склерозу и сморщиванию почек, что может явиться причиной почечной недостаточности. Местный гиалиноз, развивающийся в створках клапанов сердца при ревматизме в исходе фибриноидных изменений соединительной ткани, приводит к склерозу, деформации створок клапанов и развитию порока сердца. Таким образом, гиалиноз значительно нарушает функции органов. Вместе с тем местный гиалиноз встречается у пожилых людей как проявление инволютивных изменений.
• Виды гиалиноза — гиалиноз сосудов и гиалиноз собственно соединительной ткани. По распространенности он может быть:
- местным, например в клапанах сердца при ревматизме;
- системным, например в стенках всех артериол при гипертонической болезни.
Амилоидоз — стромально-сосудистый диспротеиноз. характеризующийся отложением в межуточной ткани, на базальных мембранах слизистых оболочек и сосудов плотного вещества — амилоида, состоящего на 96 % из аномального белка и на 4 % из полисахаридов. Механизмом образования амилоида является извращенный синтез.
В норме этот белок у человека не встречается. Накопления амилоида в строме органов приводят к атрофии их паренхимы и функциональной недостаточности. Существует много биохимически различных форм амилоида, который образуется из его предшественников в фибробластоподобных клетках (амилоидобластах) различных органов. Амилоид обладает слабыми антигенными свойствами, поэтому иммунная система не реагирует на него как на чужеродный белок, что и позволяет амилоиду накапливаться в органах и тканях.
По происхождению амилоид может быть:
- первичным (идиопатическим, т. е. невыясненного происхождения);
- вторичным, развивающимся в результате различных хронических заболеваний.
По распространенности различают амилоидоз местный и генерализованный.
Морфология.На основании биохимических и клинических данных выделяют 14 типов амилоида, связанных с извращенным синтезом иммуноглобулинов, секрета эндокринных желез, сывороточных белков и др. Амилоидоз развивается почти во всех органах и тканях, за исключением костной и хрящевой. Пораженные амилоидозом органы увеличиваются в размерах, становятся плотными, на разрезе имеют сальный вид. Нанесение на поверхность разреза таких органов растворов йода и соляной кислоты вызывает синее окрашивание ткани. На микроскопических срезах органов амилоид выявляется при окраске конго красным (конго-рот), приобретая кирпично-красный цвет. Особенно часто амилоид откладывается в строме и сосудах селезенки, почек, печени и надпочечников. В селезенке амилоид вначале появляется в лимфатических фолликулах, которые на разрезе выглядят как белесоватые зерна саго, в связи с чем такая селезенка называется «саговой» (рис. 8). Затем амилоид распространяется по всей пульпе органа, она приобретает на разрезе сальный блеск и называется «сальной» селезенкой. Большое значение в клинике имеет амилоидоз почек. Амилоидные массы вначале откладываются в стенках сосудов паренхимы почек, капилляров клубочков, затем в базальных мембранах канальцев и, наконец, в строме органа. Постепенно функциональные структуры почек полностью замещаются амилоидом, почки сморщиваются, развивается амилоидный нефроз и функция почек прекращается.

Рис. 8. «Саговая» селезенка при амилоидозе.
Прогноз при этом заболевании неблагоприятный, так как амилоидоз является необратимой дистрофией.
ЖИРОВЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Жировые стромально-сосудистые дистрофии возникают при нарушениях обмена нейтрального жира, триглицеридов или холестерина и его производных. Нейтральный жир располагается в жировых депо — подкожной жировой клетчатке, брыжейке, сальнике, эпикарде, костном мозге. Это так называемый запасный, или расходный, жир, обеспечивающий энергетические потребности организма. Стромально-сосудистые жировые дистрофии заключаются либо в избыточном накоплении нейтрального жира в жировых депо, либо в патологическом уменьшении его количества, либо в появлении жира в тех тканях, где его нет в норме. В связи с этим выделяют:
- ожирение, или тучность;
- истощение, или кахексию;
- атеро.
Ожирение — избыточное накопление жира в организме, при котором масса тела увеличивается более чем на 20—30%.
Оно дифференцируется по следующим признакам:
- по степени увеличения массы тела;
- по преимущественной локализации жировой ткани в организме.
• Оценка массы тела. В настоящее время «идеальную массу» тела оценивают с помощью «индекса массы тела» (ИМТ), предложенного Д. Гэрроу (1981). Он вычисляется по следующей формуле:
![]()
Масса тела считается нормальной при ИМТ в диапазоне 18,5— 24,9. Большие значения ИМТ свидетельствуют об избыточной массе тела (табл. 1).
• По преимущественной локализации жировой ткани выделяют:
- общее (равномерное) ожирение;
- местное ожирение — женский тип, при котором избыток подкожного жира преимущественно в области бедер и ягодиц; мужской тип, характеризующийся накоплением жира в области живота.
• По происхождению выделяют следующие виды ожирения:
- первичное, которое является результатом нарушений нейроэндокринной регуляции жирового обмена и развивается при ряде заболеваний ЦНС, сопровождающихся нейроэндокринными нарушениями — травма или опухоль головного мозга, энцефалит, поражения гипофиза и других желез внутренней секреции;
- вторичное, причиной которого могут быть избыточная калорийность пищи, пониженный уровень энергозатрат организма, что зависит от физической активности и образа жизни, индивидуальные особенности обмена веществ (в том числе липидов).
Алиментарное ожирение имеет наибольшее значение среди вторичных мезенхимальных липидозов, связано с избыточным питанием и малоподвижным образом жизни. При этом развивается ожирение сердца с отложением жира под эпикардом и между пучками мышечных волокон, особенно правых отделов сердца. Сдавленные жировой тканью мышечные волокна атрофируются, истончаются, функция миокарда снижается, иногда происходит разрыв стенки правого желудочка сердца.
Истощение — патологическое снижение массы жировой ткани. Индекс массы тела падает до 20 кг/м и ниже. При этом дефицит жировой ткани может составлять 20—25 % от ее нормального количества. Если масса тела снижается на 50 % и более по сравнению с нормой, то говорят о кахексии.
Причины истощения и кахексии:
- голодание;
- низкая калорийность пищи, не восполняющая энергозатрат организма;
- злокачественные опухоли.
Морфология. При истощении и особенно при кахексии почти полностью исчезает жир из жировых депо, при этом кожа сморщивается, подкожная клетчатка, большой и малый сальники, брыжейка приобретают охряно-желтый цвет за счет концентрации в них пигментов (красящих веществ) — липохромов. Все органы резко уменьшаются в размерах, приобретают бурый цвет, нередко покрываются слизью.
Атеро — заболевание, в развитии которого большую роль играет нарушение обмена холестерина и его производных.
УГЛЕВОДНЫЕ СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ
Углеводные стромально-сосудистые дистрофии связаны в основном с нарушением обмена глюкопротеинов и проявляются развитием в соединительной ткани, хрящах, в жировой клетчатке густой слизеподобной массы. Это так называемая слизистая дистрофии, обусловленная нарушениями функций эндокринных желез. Такая дистрофия развивается, например, при микседеме — заболевании, связанном с недостаточностью функции щитовидной железы. Ослизнение тканей может наблюдаться и при кахексии.
СМЕШАННЫЕ ДИСТРОФИИ
Смешанные дистрофии характеризуются нарушениями обмена веществ, которые проявляются одновременно в клетках и во внеклеточном матриксе. Смешанные дистрофии являются следствием нарушения обмена сложных белков и минералов.
Сложные белки — соединения, состоящие из белка и связанного с ним вещества небелковой природы.
Выделяют следующие сложные белки:
- хромопротеины — соединения, в которых белок связан с красящими веществами — пигментами;
- нуклеопротеины — комплекс белка и нуклеиновых кислот;
- липопротеины — соединения белка и липидов:
- глюкопротеины — соединения белка и углеводов.
Нарушения минерального обмена связаны с нарушениями метаболизма солей и их ионов.
СМЕШАННЫЕ БЕЛКОВЫЕ ДИСТРОФИИ
Смешанные белковые дистрофии характеризуются нарушениями обмена сложных белков, главным образом нарушениями метаболизма хромопротеинов, или эндогенных пигментов.
Выделяют три группы хромо протеинов:
- гемоглобиногенные пигменты;
- протеиногенные (тирозиновые) пигменты;
- липидогенные пигменты.
Патогенез нарушений обмена пигментов может заключаться в изменении их количества
- увеличении, уменьшении или в полном отсутствии;
- распространенности (местные или общие);
- появлении аномальных пигментов, не встречающихся в норме.
Нарушения обмена гемоглобиногенных пигментов, связанных с обменом гемоглобина.
Физиологические функции этих пигментов заключаются в транспорте и депонировании кислорода и железа, в транспорте углекислого газа, электронов и др.
В организме постоянно происходит гемолиз (распад) эритроцитов, в результате чего их красящее вещество — гемоглобин — распадается на белок — глобин, и протопорфирин железа — гем. Железо либо сохраняется в геме, либо покидает его. Таким образом, уже в норме появляются две группы гемоглобиногенных пигментов: железосодержащие и не содержащие железа.
Железо, вышедшее из гема, соединяется с цитоплазмой клеток ретикулоэндотелиальной системы (РЭС) и макрофагов, образуя четыре пигмента, два из которых возникают только в условиях патологии:
- гелюсидерин — образуется как в норме, так и в условиях патологии;
- ферритин — образуется как в норме, так и в условиях патологии;
- солянокислый гелютин — образуется при желудочных кровотечениях;
- лилярийный пигмент (гемомеланин) — образуется при малярии.
Гем. лишенный железа, образует три пигмента:
- билирубин;
- стеркобилин;
- уробилин.
Патогенез. В условиях патологии (при некоторых инфекциях, интоксикациях, переливании несовместимой крови, анемиях, переохлаждении организма, при ожоговой болезни и др.) резко усиливается внутрисосудистый гемолиз эритроцитов и в избытке образуются гемоглобиногенные пигменты. Гемоглобин захватывается эндотелиальными клетками интимы сосудов, ретикулярными клетками, гистиоцитами селезенки, печени, костного мозга, лимфатических узлов, макрофагами и эпителиальными клетками легких. почек. В этих клетках гем соединяется с мукополисахаридами цитоплазмы и образуются гемосидерин и ферритин. Эти пигменты придают органам ржаво-коричневую окраску, что характеризует общий (распространенный) гемосидероз.
Если разрушение эритроцитов происходит после их выхода из сосудов, например при кровоизлияниях в ткани, возникает местный гемосидероз. При этом гемосидерин захватывается в основном макрофагами, в которых образуются гемосидерин и ферритин, и такие макрофаги называются сидерофагами. Они выявляются в тканях с помощью реакции Перлса — реакции образования берлинской лазури (железосинеродистой соли трехвалентного железа), при которой все клетки и внеклеточные скопления гемосидерина, а также других гемоглобиногенных пигментов, содержащих железо, окрашиваются в голубой цвет. В клинике большое значение имеет местный гемосидероз легких — так называемая бурая индурация легких.
В условиях патологии могут появляться еще два железосодержащих гемоглобиногенных пигмента, не встречающихся в норме:
- солянокислый гематин;
- малярийный пигмент.
Солянокислый гематин имеет бурый цвет и образуется в желудке при соединении соляной кислоты желудочного сока с гемоглобином при желудочных кровотечениях, которые могут возникать при язвенной болезни желудка, эрозивных гастритах, распаде опухолей желудка. При этом возникает рвота «кофейной гущей» из-за содержания в рвотных массах солянокислого гематина. Малярийный пигмент (гемомеланин) появляется в циркулирующей крови при распаде эритроцитов, пораженных малярийным плазмодием. Гемомеланин захватывается клетками РЭС, в результате чего ткани селезенки, печени, костного и головного мозга, мозговых оболочек, лимфатических узлов приобретают пепельную окраску. Развивается распространенный гемосидероз.
В физиологических условиях при распаде эритроцитов и потере гемом железа в результате сложных биохимических реакций в печени образуется не содержащий железа пигмент билирубин, входящий в состав желчи и придающий ей желтовато-зеленый цвет. Попадая вместе с желчью в кишечник, под влиянием ферментов кишечного сока билирубин превращается в стеркобилин и окрашивает каловые массы, а попадая вместе с кровью в почки и затем в мочу, превращается в уробилин, обусловливающий ее окраску.
При нарушении образования билирубина в печени или при нарушении его выделения из нее билирубин накапливается в крови и окрашивает все ткани в желтый цвет. Развивается желтуха (см. главу 17).
НАРУШЕНИЯ ОБМЕНА ПРОТЕИНОГЕННЫХ ПИГМЕНТОВ
Основными функциями протеиногенных пигментов являются рецепция света, защита от ультрафиолетового излучения, синтез и депонирование биологически активных веществ. Наибольшее значение в патологии имеют следующие протеиногенные пигменты: меланин, пигмент гранул энтерохромаффинных клеток, адренохром.
Меланин — пигмент коричнево-черного цвета, образующийся при окислении тирозина в клетках-меланобластах при участии фермента тирозиназы.
Обмен меланина регулируется вегетатив-нои нервной системой, гипофизом, надпочечниками, половыми железами. В норме меланин содержится в радужке глаз, волосах, коже, пищеварительном тракте, твердой мозговой оболочке, обусловливая их окраску. При избыточном ультрафиолетовом облучении меланин накапливается в коже, придавая ей коричневый оттенок, называемый загаром.
Патогенез. Патологическое усиление образования меланина называется меланозом, который может быть общим и местным. Общий меланоз развивается в коже при кахексии, тяжелых авитаминозах, туберкулезном или опухолевом поражении надпочечников. В последнем случае развивается бронзовая, или аддисонова, болезнь, при которой кожные покровы приобретают бронзовый оттенок (рис. 9). К местным меланозам относятся так называемые родимые пятна,или невусы. на коже. Из невусных клеток может развиться злокачественная опухоль — меланома.
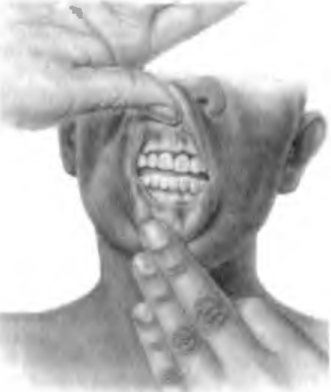
Рис. 9. Меланодермия и пигментация слизистой оболочки полости рта при аддисоновой болезни.
Наследственное отсутствие меланина — альбинизм характеризуется отсутствием пигмента в коже, волосах, радужке глаз. Люди и животные, страдающие альбинизмом, называются альбиносами — у них очень белая кожа, белые волосы, а радужки глаз красные. Локальное отсутствие меланина в виде разной формы очагов может наблюдаться после воспалительных заболеваний кожи и носит название лейкодерма.
Пигмент гранул энтерохромаффшных клеток, входящих в состав APUD-системы, или диффузной эндокринной системы организма, участвует в образовании биологически активных веществ — серотонина, гастрина и др.
Адренохром — темно-коричневый пигмент клеток мозгового вещества надпочечников, образуется при окислении адреналина. Опухоли из этих клеток называются феохромоцитомами и имеют своеобразную клиническую картину.
НАРУШЕНИЯ ОБМЕНА ЛИПИДОГЕННЫХ ПИГМЕНТОВ
Среди липидогенных пигментов основное значение имеет липофусцин и его разновидности — гемофусцин, цероид, липохромы. Липофусцин представляет собой сложное соединение, в котором преобладают жиры; он образуется в клетках печени, сердца, почек, скелетных мышц, симпатических ганглиев в виде мелких золотисто-коричневых гранул. Внутриклеточные скопления липофусцина не оказывают влияния на функции клеток: этот пигмент накапливается в них при старении организма, при истощающих заболеваниях — алиментарной и опухолевой кахексии, гнойно-резорбтивной лихорадке, некоторых инфекциях. Поэтому липофусцин иногда называют «пигментом старения», или «пигментом изнашивания». Избыточное накопление липофусцина в клетках называется липофусцинозом.
НАРУШЕНИЯ ОБМЕНА НУКЛЕОПРОТЕИНОВ
Нуклеопротеины — вещества, состоящие из белка, соединенного либо с нуклеиновыми кислотами, либо с пуриновыми основаниями. Наибольшее значение в патологии нуклеопротеинов имеют дезоксирибонуклеиновая кислота (ДНК), рибонуклеиновая кислота (РНК) и пуриновые основания.
ДНК является основой хромосом и содержится в клеточном ядре, а РНК — переносчик генетической информации и располагается в ядрышках и цитоплазме клеток. При распаде нуклеопротеинов, помимо белка и ряда других соединений, образуются пуриновые основания, превращающиеся в мочевую кислоту, которая выделяется с мочой. При заболеваниях, сопровождающихся интенсивным распадом ядер клеток (гнойные воспалительные процессы, лейкозы и др.), возрастает содержание мочевой кислоты в крови — гиперурикемия и как следствие в моче — гиперурикурия. На содержание в организме и метаболизм мочевой кислоты оказывает влияние богатая пуринами пища — мясо, яйца, икра. При нарушениях обмена нуклеопротеинов может развиться ряд заболеваний, среди которых наибольшее значение имеет подагра.
Подагра.
В развитии заболевания определенную роль играет наследственная предрасположенность, а также употребление пищи, содержащей большое количество животных белков.
Патогенез. Болезнь заключается в повышенном образовании солей мочевой кислоты, что проявляется гиперурикемией и гиперурикурией. При этом периодически происходит выпадение кристаллов мочекислого натрия в синовиальных оболочках и хрящах мелких суставов, в основном пальцев рук и ног, но могут поражаться и голеностопные, и коленные суставы, сухожилия мышц, хрящи ушных раковин.
Морфология. Ткани в области выпадения кристаллов некротишруются, что сопровождается резкой болью. Вокруг очагов некроза и скоплений кристаллов мочекислых солей развивается продуктивное воспаление, завершающееся образованием рубцовой соединительной ткани. Повторяющиеся атаки подагры приводят к массивному развитию соединительной ткани и формированию так называемых подагрических шишек (tophi unci). При этом происходит деформация суставов. В почках кристаллы мочевой кислоты накапливаются в канальцах и собирательных трубках, в ответ на это развивается хроническое воспаление и атрофия почечной ткани — подагрические почки.