Жировые дистрофии связаны с избыточным накоплением в цитоплазме паренхиматозных клеток липидов (нейтральных жиров, триглицеридов, фосфолипидов, холестерина), либо с появлением их в тех клетках, где они в норме не встречаются, либо с появлением в цитоплазме клеток липидов аномального состава. Потребность человека в жирах составляет 80—100 г в сутки.
Основные функции липидовв организме:
- структурная — липиды составляют основу клеточных мембран;
- регулирующая;
- энергообеспечивающая, поскольку липиды являются одним из главных источников энергии.
В зависимости от клинических проявлений выделяют:
- липидозы;
- ожирение;
- истощение.
Причинами приобретенных липидозов наиболее часто служат гипоксия и различные интоксикации. Поэтому жировые дистрофии являются компонентом заболеваний, сопровождающихся ки-i слородным голоданием. — ишемической болезни сердца, гипертонической болезни, пороков сердца, хронических заболеваний легких (бронхоэктатическая болезнь, туберкулез, эмфизема легких). приводящих к развитию легочно-сердечной недостаточности. Кроме того, жировую дистрофию вызывают различные инфекции и интоксикации, которые сопровождаются как гипоксией, так и блокадой токсинами ферментов, катализирующих в клетках метаболизм липидов. Липидозы иногда могут быть связаны с недостатком витаминов и некоторых аминокислот.
В патологии наибольшее значение имеют жировые дистрофии миокарда, печени и почек.
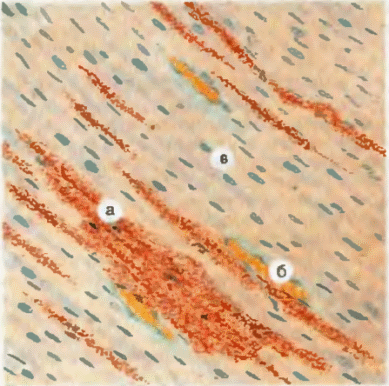
Рис. 3. Жировая дистрофия миокарда. а — кардиомиоциты с жировым включениями; б — венулы; в — кардиомиоциты, свободные от жировых включений.
Жировая дистрофия миокарда развивается путем декомпозиции жиробелковых комплексов мембран внутриклеточных структур, а также в результате инфильтрации кардиомиоцитов липидами. Вне зависимости от механизма дистрофии в клетках миокарда вначале появляются мелкие включения жира (пылевидное ожирение), затем они сливаются в капли (мелкокапельное ожирение), которые постепенно заполняют всю саркоплазму и могут приводить к гибели клеток (рис. 3).
на для резкого снижения функции сердца и развития сердечной недостаточности.
Жировая дистрофия печени, или жировой гепатоз
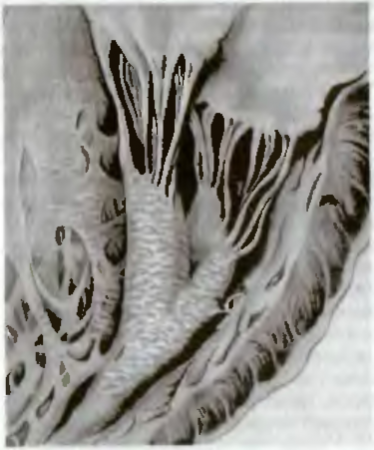
Рис. 4. Жировая дистрофия миокарда («тигровое сердце»). Под эндокардом видны желто-белые полоски, соответствующие участкам включения липидов в кардиомиоцитах.
Вместе с тем при многих интоксикациях и инфекциях возможен механизм декомпозиции мембран внутриклеточных структур с распадом их жиробелковых комплексов. Наконец, жировой гепатоз развивается в результате трансформации белков и углеводов в липиды, что наблюдается, например, при хронической алкогольной интоксикации. В любом случае в цитоплазме гепатоцитов, в основном периферии печеночных долек, развивается вначале пылевидное ожирение, которое трансформируется в мелкокапельное, а затем — в крупнокапельное. При этом ядро и внутриклеточные структуры оттесняются на периферию клеток, которые нередко гибнут. В этих случаях жировые включения погибших гепатоцитов сливаются, образуя жировые кисты. Макроскопические изменения печени зависят от степени выраженности дистрофии. В тяжелых случаях, например при алкоголизме, печень увеличена в размере, дряблая, на разрезе охряного цвета — «гусиная печень». При менее выраженной жировой дистрофии печень также увеличена в размере, на разрезе желтовато-серого цвета. При жировых гепатозах функция печени долго сохраняется, однако по мере прогрессирования основного заболевания и жировой дистрофии она снижается, иногда весьма значительно.
Жировая дистрофия почек развивается путем инфильтрации эпителия канальцев при гиперлипидемии, наблюдающейся, в частности, при нефротическом синдроме. В этой ситуации липиды оказываются в первичной моче (гиперлипидурия) и усиленно реабсорбируются клетками эпителия канальцев, но в таких больших количествах, что эти клетки не способны метаболизировать попавшие в них липиды — развивается мелкокапельное ожирение эпителия канальцев. Обычно оно сочетается с их гиалиново-капельной дистрофией. Почки при этом внешне изменены мало, но при тяжелом течении основного патологического процесса они приобретают серовато-желтый цвет, а на разрезе их пирамиды могут принимать желтую окраску.
Исход паренхиматозной жировой дистрофии зависит от степени ее выраженности — пылевидное и мелкокапельное ожирение обратимо при ликвидации вызвавшей его причины, крупнокапельное ожирение может закончиться гибелью клеток.
ВРОЖДЕННЫЕ ПАРЕНХИМАТОЗНЫЕ ЛИПИДОЗЫ
Врожденные паренхиматозные липидозы являются наследственными ферментопатиями, наследуемыми по аутосомно-рецессивному типу, и характеризуются накоплением в клетках липидов, повреждающих структуры клеток и сопровождающихся нередко гибелью самих клеток. Наиболее часто встречаются следующие липидные тезаурисмозы:
- Болезнь Гоше вызвана отсутствием фермента бета-глюкоцереброзидазы. В результате глюкоцереброзиды накапливаются в печени, селезенке, костном мозге, в головном мозге, эндокринных железах и лимфатических узлах, что приводит к гибели клеток этих органов и к прогрессирующему слабоумию, увеличению массы печени, селезенки и истощению (кахексии).
- Болезнь Нимана—Пика развивается при отсутствии фермента сфингомиелиназы, расщепляющей сфингомиелин, входящий в состав многих тканей, но особенно нервной ткани. У больных детей он накапливается в клетках большинства органов и при этом происходит увеличение массы печени и селезенки (гепато- и спленомегалия), отставание в психическом развитии, появляются неврологическая симптоматика, гипотония, истощение. Дети погибают в возрасте 2—3 лет.
УГЛЕВОДНЫЕ ДИСТРОФИИ
Углеводные дистрофии связаны с накоплением в клетках бел-ково-полисахаридных комплексов (гликоген, гликопротеины), либо с образованием этих веществ в тех клетках, где их нет в норме, либо с изменением их химического состава.
Углеводы — обязательный и наиболее значительный компонент пищи. В сутки человек потребляет 400—600 г различных углеводов. Они являются необходимым элементом метаболизма, важным компонентом структуры клеток и межклеточного вещества и одним из главных источников энергии для обеспечения жизнедеятельности организма.
ПРИОБРЕТЕННЫЕ УГЛЕВОДНЫЕ ДИСТРОФИИ
Гипогликемии — состояния, характеризующиеся снижением содержания глюкозы в крови ниже 65 мг%, или 3,58 ммоль/л. В норме уровень глюкозы крови натощак колеблется в диапазоне 65—110 мг%, или 3,58—6,05 ммоль/л.
Причинами гипоглюкемии являются заболевания печени — xpонические гепатиты, циррозы печени, ее жировая дистрофия, а также длительное голодание.
Результаты заболеваний:
- нарушение транспорта глюкозы из крови в гепатоциты, снижение уровня образования в них гликогенеза и в связи с этим отсутствие депонированного гликогена;
- торможение процесса образования гликогена и транспорта глюкозы из гепатоцитов в кровь.
Последствия гипогликемии
- Гипогликемический синдром — стойкое снижение содержания глюкозы в крови ниже нормы (до 60—50 мг%, или 3,3—2,5 ммоль/л), приводящее к расстройству жизнедеятельности организма.
- Гипогликемическая кома — состояние, характеризующееся:
- — падением концентрации глюкозы в крови ниже 40—30 мг%, или 2.0—1.5 ммоль/л);
- — потерей сознания;
- — опасными для жизни расстройствами функций организма.
Гипергликемии — состояния, характеризующиеся увеличением
содержания глюкозы в крови выше нормы (более 120 мг%, или 6,05 ммоль/л натощак).
Причины гипергликемии:
- патология эндокринной системы, сопровождающаяся избытком гормонов, стимулирующих поступление углеводов в кровь (глюкагона, глюкокортикоидов, катехоламинов, тиреоидных гормонов, соматотропного гормона) либо недостатком инсулина или снижением его эффективности;
- нейро- и психогенные расстройства, например реактивные психозы, стресс-реакции и подобные им состояния, характеризующиеся активацией органов эндокринной системы;
- переедание, прежде всего длительное избыточное потребление кондитерских изделий;
- заболевания печени, при которых гепатоциты теряют cпособность трансформировать глюкозу в гликоген.
Последствия
- Гипергликемический синдром — состояние сопровождающееся значительным увеличением содержания глюкозы в крови выше нормы (до 190—210 мг%, 10,5—11,5 ммоль/л и более), приводящее к расстройствам жизнедеятельности организма.
- Гипергликемическая кома, характеризующаяся потерей сознания, снижением или утратой рефлексов, расстройствами дыхания и кровообращения, нередко заканчивающаяся смертью больного.
Наиболее часто гипергликемия наблюдается при сахарном диабете, развивающемся в результате абсолютной или относительной инсулиновой недостаточности (см. главу 19).
НАСЛЕДСТВЕННЫЕ УГЛЕВОДНЫЕ ДИСТРОФИИ (ГЛИКОГЕНОЗЫ)
Гликогенозы — типовая форма патологии углеводного обмена наследственного генеза, характеризующаяся накоплением гликогена в клетках, что обусловливает нарушение жизнедеятельности организма.
Главная причина — наследуемая или врожденная аномалия генов, кодирующих синтез ферментов расщепления (реже — образования) гликогена. Наследуются по аутосомно-рецессивному типу. Выделяют более 10 типов гликогенозов. Среди них наиболее часто встречаются болезни Гирке. Помпе, фетальный муковисцилоз, а также болезни Форбса—Кори, Андерсена, Мак-Ардла.
Болезнь Гирке возникает при отсутствии фермента глюкозо-6-фосфатазы, что приводит к накоплению гликогена в клетках печени и почек, но к отсутствию углеводов в крови. Это сопровождается вторичным гипофизарным ожирением. Большинство детей погибают от ацидотической комы.
Болезнь Помпе связана с отсутствием кислой альфа- 1,4-глюкозидазы в лизосомах, что приводит к накоплению гликогена в сердце, поперечнополосатых и гладких мышцах, в том числе в межреберных, диафрагмальных, в мышцах языка, пищевода, желудка и т.п. Дети погибают в раннем возрасте от сердечной или дыхательной недостаточности.
Остальным муковисцидоз — заболевание, связанное с генотипической ферментопатией. приводящей к нарушению обмена мукоидов, входящих в секрет многих желез. В результате секрет желез становится вязким и густым, выводится с трудом, что приводит к растяжению желез, превращению их в кисты, особенно в поджелудочной железе, слизистых оболочках желудочно-кишечного тракта и дыхательных путей, слюнных, потовых, слезных железах и др. При этом в легких часто развиваются ателектазы с развитием пневмонии и бронхоэктазов. Смерть наиболее часто наступает от легочно-сердечной недостаточности.