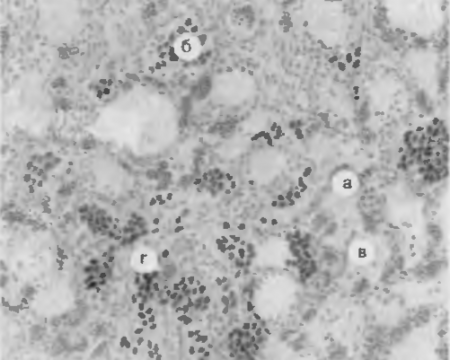
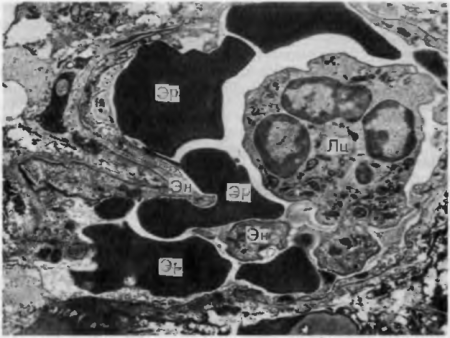
Кровообращение условно разделяют на центральное и периферическое.
Центральное кровообращение, осуществляясь на уровне сердца и крупных сосудов, обеспечивает:
- поддержание системного давления крови;
- направление движения крови из артериального русла в венозное и далее — в сердце;
- демпфирование (амортизацию) систолических и диастолических колебаний артериального давления при выбросе крови из желудочков сердца для обеспечения равномерного кровотока.
Периферическое (регионарное) кровообращение осуществляется в сосудах органов и тканей. К нему относится кровообращение в сосудах микроциркуляторного русла, которое включает:
- артериолы;
- прекапилляры;
- капилляры;
- посткапилляры;
- венулы:
- артериоловенулярные шунты.
Микроциркуляторное русло обеспечивает доставку крови к тканям, транскапиллярный обмен субстратами метаболизма, кислородом. углекислым газом, а также транспорт крови от тканей. Артериоловенозные шунты определяют объем крови, притекающей к капиллярам. При закрытии этих шунтов кровь из артериол поступает в капилляры, а при открытии — в венулы, минуя капилляры.
Лимфатическая система структурно и функционально объединена с системой кровообращения и обеспечивает лимфообразующую, дренажную, барьерную, дезинтоксикационную, кровообразующую функции и включает:
- лимфатические органы — лимфатические узлы, лимфатические фолликулы, миндалины, селезенку;
- лимфатические транспортные пути — капилляры, микро- и макрососуды, синусы, которые имеют адренергическую иннервацию. общую с кровеносными сосудами.
Все компоненты системы кровообращения тесно связаны между собой, и расстройство деятельности одного из них, например центрального, приводит к изменениям и периферического, и микроциркуляторного кровообращения. С другой стороны, расстройства системы микроциркуляции могут стать причиной или усугублять нарушения функции сердца или крупных сосудов. При этом большую роль в патологии играет тесная интеграция кровеносной системы с лимфатической, которая по существу также составляет систему микроциркуляции. Лимфа образуется в лимфатических капиллярах из тканевой жидкости и по лимфатическим сосудам транспортируется в венозную систему. При этом 80—90 % тканевого фильтрата оттекает в венозное, а 10—20 % — в лимфатическое русло. Отток лимфы и венозной крови обеспечивается одними и теми же механизмами — присасывающим действием сердца, грудной клетки, диафрагмы и работой мышц.
ВИДЫ РАССТРОЙСТВ КРОВООБРАЩЕНИЯ
Выделяют нарушения центрального и периферического кровообращения.
Патология центрального кровообращения обусловлена главным образом нарушениями функций сердца или тока крови в крупных сосудах — аорте, нижней и верхней полых венах, легочном стволе, легочных венах. При этом возникает недостаточность кровообращения, которая сопровождается изменениями периферического кровообращения, в том числе и микроциркуляции. В результате органы и ткани не получают достаточного количества кислорода и других метаболитов, из них не удаляются токсичные продукты метаболизма. Причиной этих нарушений может быть либо нарушение функции сердца, либо снижение сосудистого тонуса—гипотония.
Патология периферического (регионарного) кровообращения, включая нарушения микроциркуляции, проявляются в трех основных формах:
- нарушения кровонаполнения (артериальное полнокровие и малокровие, венозное полнокровие);
- нарушения реологических свойств крови (тромбоз, эмболия, стаз, ДВС-синдром);
- нарушения проницаемости стенок сосудов (кровотечения, кровоизлияния, плазморрагия).
Полнокровие сосудов (гиперемия) может быть артериальным и венозным. Каждое из них в свою очередь может быть:
- по течению — острым и хроническим;
- по распространенности — местным и общим.
ПОЛНОКРОВИЕ
Артериальное полнокровие (гиперемия) обусловлено увеличением притока крови в систему микроциркуляции при нормальном ее оттоке по венам, что проявляется расширением артериол, повышением внутрисосудистого давления и местной температуры тканей.
Причиной общей артериальной гиперемии может быть увеличение объема циркулирующей крови (плетора) или количества эритроцитов (эритремия); местной артериальной гиперемии — различные физические (температурные), химические (щелочи, кислоты), биологические (инфекционной и неинфекционной природы) факторы, воспаление, а также нарушение иннервации (ангионевротическая гиперемия) и психогенные воздействия: например, слово может привести к артериальной гиперемии лица и шеи, проявляющейся «краской стыда или гнева».
Механизмы развития артериального полнокровия:
- нейрогенный механизм связан с преобладанием парасимпатических эффектов на артериолы и капилляры над симпатическими влияниями, что наблюдается, например, при травме, сдавлении опухолью или воспалении регионарных парасимпатических ганглиев, а также симпатических ганглиев или нервных окончаний;
- гуморальный механизм обусловлен увеличением либо уровня биологически активных веществ с сосудорасширяющим действием (кининов, простагландинов, серотонина), либо повышением чувствительности к ним стенок артериол (в частности, к ионам внеклеточного калия);
- нейромиопаралитический механизм заключается в истощении запасов катехоламинов в симпатических нервных окончаниях или в снижении тонуса мышечных волокон в стенках артериол, что может быть вызвано длительным физическим воздействием (например, при применении грелок, горчичников, медицинских банок), изменениями барометрического давления и др.
Виды артериального полнокровия.
Физиологическая артериальная гиперемия возникает при интенсивном функционировании органа, например в работающих мышцах, беременной матке, в стенке желудка после приема пищи. Она обеспечивает усиленное поступление в ткани кислорода и питательных веществ и способствует удалению продуктов их распада.
Патологическая артериальная гиперемия не связана с усилением функции органа, развивается при воспалении, нарушениях иннервации органов, травмах тканей, эндокринных заболеваниях, значительном повышении артериального давления и др.
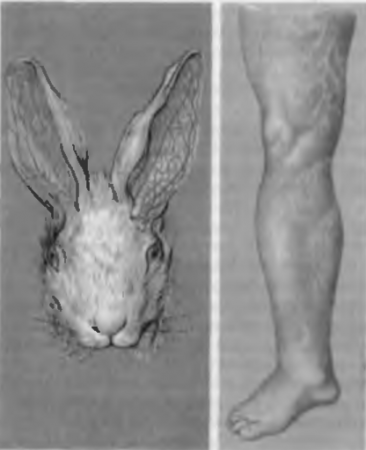
Рис. 14. Полнокровие сосудов. а — артериальная гиперемия; б — венозная гиперемия; расширение и переполнение кровью вен бедра и голени.
При этом стенки артериол могут разрываться и возникает кровотечение или кровоизлияние в ткани.
Признаки артериального полнокровии
При артериальной гиперемии увеличивается пульсация артерий, меняется микроциркуляторное русло — расширяются артериолы, раскрываются резервные капилляры, в них увеличивается скорость кровотока, повышается кровяное давление. Гиперемия хорошо видна на поверхности кожи (рис. 14, а).
При артериальной гиперемии отмечаются:
- увеличение числа и диаметра артериальных сосудов;
- покраснение органа ткани или их участков;
- повышение температуры тканей в области их гиперемии;
- увеличение объема и напряжения (тургора) органа или ткани в связи с увеличением их кровонаполнения;
- увеличение лимфообразования и лимфооттока, что обусловлено повышением перфузионного давления в сосудах микроциркуляции.
Венозное полнокровие (гиперемия) обусловлено затруднением оттока крови по венам при нормальном ее притоке по артериям, что приводит к увеличению кровонаполнения органа или ткани. Причиной венозного полнокровия является препятствие оттоку
крови в результате закрытия просвета вены тромбом или эмболом. при сдавлении вен опухолью, рубцом, жгутом, при врожденном недоразвитии эластического каркаса стенок вен или их клапанного аппарата, а также при развитии сердечной недостаточности.
Признаки венозного полнокровия:
- цианоз, т. е. синюшный оттенок слизистых оболочек, кожи, ногтей и органов из-за увеличения в них количества венозной крови, бедной кислородом;
- снижение температуры тканей вследствие падения вних интенсивности обмена веществ;
- отек тканей, развивающийся в результате гипоксии (кислородного голодания) тканей стенок сосудов микроциркуля-торного русла, повышения их проницаемости и выхода в окружающую ткань плазмы крови;
- увеличение объема органов и тканей из-за скопления в них венозной крови и отека.
Местное венозное полнокровие имеет значение в патологии главным образом в связи с развивающимся при этом острым отеком тканей в том или ином регионе тела, а также с возможностью возникновения инфаркта селезенки при тромбозе селезеночной вены. При хроническом местном венозном (застойном) полнокровии в органе активизируется образование фибробласта-ми коллагена и в строме разрастается соединительная ткань — развивается органа.
Общее венозное полнокровие имеет большое значение в патологии, возникает при различных заболеваниях и может иметь тяжелые последствия.
Острое общее венозное полнокровие чаще развивается при острой сердечной недостаточности (острый инфаркт миокарда, острый миокардит), а также в атмосфере с низким содержанием кислорода (например, при разгерметизации кабины самолета, высоко в горах, при недостаточном поступлении кислорода из акваланга при подводных работах и т. п.). При этом в тканях быстро нарастают гипоксия и ацидоз (закисление). повышается сосудистая проницаемость, появляется и прогрессирует отек, часто сопровождающийся периваскулярными кровоизлияниями.
Хроническое общее венозное полнокровие обычно развивается при хронических заболеваниях сердца, заканчивающихся хронической сердечной недостаточностью (хроническая ишемическая болезнь сердца, пороки сердца, кардиомиопатии). Помимо всех тех изменений, которые характеризуют острую венозную гиперемию, при хроническом венозном полнокровии постепенно развиваются атрофия паренхимы органов и их стромы, в результате чего происходит уплотнение (индурация) органов и тканей. Кроме того, хронический отек и плазморрагия вызывают перегрузку лимфатической системы и развитие ее недостаточности. Формируется капиллярнотрофическая недостаточность, которая характеризуется:
- ом микрососудов, уменьшением их просветов и уменьшением количества капилляров, что обусловливает уменьшение кровотока по капиллярам, транскапиллярный обмен веществ и нарастание кислородного голодания;
- преобразованием истинных капилляров в емкостные (депонирующие), в которых эритроциты располагаются не в один, а в несколько рядов, капилляры резко расширяются и превращаются в венулы, стенки их теряют тонус, что приводит к еще большему расширению капилляров и венул и усиливает венозную гиперемию. При этом количество истинных капилляров снижается, артериальная кровь попадает в венозную систему по коляатералям (обходным сосудам), что способствует нарастанию гипоксических и метаболических изменений в тканях.
Характерные изменения в органах и тканях, которые развиваются при хроническом общем венозном полнокровии.
- В коже и подкожной клетчатке, особенно нижних конечностей, происходит расширение венозных сосудов, отек кожи и подкожной клетчатки (анасарка), атрофия кожи, застой лимфы в лимфатических сосудах (лимфостаз). На фоне хронического венозного полнокровия часто развиваются трофические язвы голеней и стоп (рис. 14, б).
- В легких длительный венозный застой имеет особое значение в связи с тем, что он развивается при хронической сердечной недостаточности (см. главу 13). При этом в легочных венах, впадающих в левое предсердие, развивается застой крови, что способствует прогрессирующей гипоксии. При этом повышается проницаемость стенок сосудов и из венул и капилляров в окружающую ткань выходит сначала плазма крови, а затем и эритроциты. Последние захватываются макрофагами, в которых гемоглобин превращается в гемосидерин и ферритин, а макрофаги получают название сидерофагов. Часть макрофагов альвеол, загруженных гемосидерином, попадает в бронхи и вместе с мокротой выводится из организма. В мокроте они называются «клетками сердечных пороков«. Часть сидерофагов распадается в строме легких, чему способствует нарастающая недостаточность лимфатических сосудов, перегруженных отечной жидкостью, сидерофагами и гемосидерином. Постепенно развивается застой лимфы. Прогрессирующие гипоксия и застой лимфы являются стимулами для активизации системы фибробластов в ткани легких и интенсивного образования ими коллагена. Нарастает склероз легких, они становятся плотными, развивается их индурация (от лат. durum — плотный). При этом гемосидерин, образующий скопления в строме и в альвеолах и характеризующий местный гемосидероз, придает легким бурый цвет и развивается бурая индурация легких — необратимое состояние, значительно ухудшающее течение хронической сердечной недостаточности и общее состояние больного (рис. 15).
- В печени хроническая венозная обычно также является следствием хронической сердечной недостаточности и декомпенсации сердца. При этом застой крови вначале происходит в нижней полой вене, затем в венах печени и в центральных венах печеночных долек. Центральные вены расширяются, через их стенки выходит плазма крови и эритроциты и в центре долек атрофируются гепатоциты. На периферии дольки гепатоциты подвергаются жировой дистрофии и ткань печени на разрезе становится пестрой, напоминающей мускатный орех — на желто-коричневом фоне отчетливо видны красные точки в центрах долек. Такая картина носит название «мускатной печени» (рис. 16).
- Селезенка при венозном застое увеличивается в размерах (застойная спленомегалия), становится синюшной и плотной (цианотическая индурация селезенки), на разрезе не дает соскоба пульпы, ее фолликулы атрофичны, а красная пульпа склерозирована.
МАЛОКРОВИЕ
Артериальное малокровие, или ишемия, — уменьшение кровенаполнения органа или ткани, обусловленное либо снижением притока к ним крови по артериям, либо значительным увеличением потребности тканей в кислороде и субстратах метаболизма, что приводит к несоответствию между потребностями тканей в кровоснабжении и возможностями артериального кровотока. В зависимости от причин и механизмов развития ишемии выделяют пять разновидностей артериального малокровия: ангиоспастическое, обтурационное, компрессионное, в результате острого перераспределения крови и дисфункциональное.
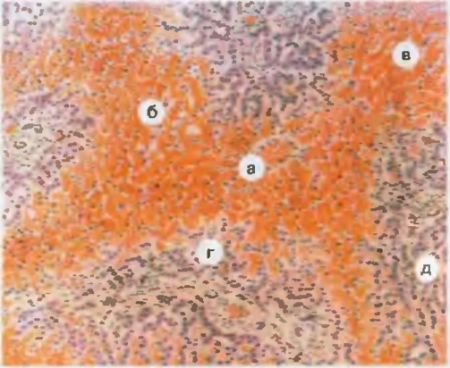
Рис. 16. Хроническое венозное полнокровие печени (мускатная печень). В центре долек центральные вены и синусоиды резко расширены, полнокровны (а), печеночные клетки атрофичны (б), в области кровоизлиянии (в) разрушены. По периферии долек печеночные балки сохранены (г), перисинусоидальные пространства расширены (д).
Ангиоспастическое малокровие обусловлено спазмом артерий вследствие увеличения содержания в тканях веществ, вызывающих спазм сосудов (например, ангиотензин, вазопрессин, катехоламины и т. п.), или повышением чувствительности к ним стенок артериол (при увеличении содержания в них ионов кальция или натрия), а также при преобладании симпатико-адреналовых влияний над парасимпатическими (стресс, стенокардия, аппендикулярная колика).
Обтурационное малокровие развивается при полном или частичном закрытии просвета артерии тромбом, эмболом (при остром малокровии) или атеросклеротической бляшкой (при хронической ишемии).
Компрессионное малокровие возникает при остром или хроническом сдавлении сосуда извне — жгутом, опухолью, отечной тканью и т. п.
Малокровие в результате острого перераспределения крови наблюдается при быстром притоке крови в ранее ишемизированные ткани. Например, при быстром удалении асцитической жидкости, сдавливавшей сосуды брюшной полости, в эту область устремляется кровь и возникает ишемия сосудов головного мозга.
Дисфункциональное малокровие является следствием значительного повышения тканями расхода кислорода и субстратов метаболизма при резкой интенсификации функции органа, например ишемия миокарда при внезапной интенсивной нагрузке на сердце (бег, поднятие тяжестей, тяжелая физическая работа), ишемия мышц голени у пожилых людей при быстрой ходьбе и т. п. Обычно этот вид ишемии возникает при сужении просвета снабжающей артерии атеросклеротической бляшкой.
По характеру течения ишемия может быть острой и хронической.
Признаки ишемии:
- побледнение ткани и органа из-за снижения их кровенаполнения и числа функционирующих капилляров;
- снижение пульсации артерий и уменьшение их диаметра в результате уменьшения их диастолического наполнения кровью и падения артериального давления:
- понижение температуры ишемизированной ткани вследствие уменьшения притока теплой артериальной крови и снижения интенсивности метаболизма в ишемизированном регионе;
- замедление тока крови по микрососудам вплоть до ее остановки;
- снижение лимфообразования в результате падения перфузионного давления в сосудах микроциркуляции.
Последствия и значение ишемии.
Кислородное голодание тканей (гипоксия) является главным патогенным фактором ишемии. Развивающиеся при этом изменения связаны с продолжительностью и тяжестью гипоксии, чувствительностью к ней органов и наличием коллатерального кровообращения в ишемизированной ткани. Наиболее чувствительны к гипоксии головной мозг, почки и миокард, в меньшей степени — легкие и печень, в то время как соединительная, костная и хрящевая ткани отличаются максимальной устойчивостью к недостатку кислорода.
Ишемия способствует распаду в клетках макроэргических соединений — креатинфосфата и АТФ, что компенсаторно активизирует бескислородный (анаэробный) путь окисления и образования энергии — анаэробный гликолю. Следствием этого является накопление в тканях недоокисленных продуктов метаболизма, что приводит к ацидозу тканей, усилению перекисного окисления липидов, стимуляции гидролитических ферментов лизосом и в итоге — к распаду мембран клеток и внутриклеточных структур. Возникающий энергетический дефицит способствует, кроме того, накоплению в клетках ионов кальция, активизирующих ряд ферментов, которые также приводят клетки к гибели.
Функциональное состояние органа имеет большое значение при ишемии: чем интенсивнее он функционирует, тем больше нуждается в притоке артериальной крови и тем чувствительнее к малокровию.
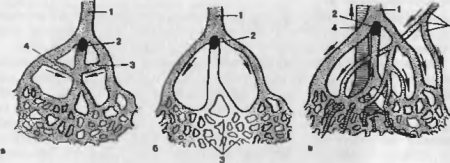
Рис. 17. Схема развития коллатерального кровообращения и образования инфарктов (по Я. Л. Рапопорту). а — схема достаточных коллатералей: артерия (1) разделялся на три ветви, из которых одна (2) закупорена; питаемая ею область получает достаточное количество крови по коллатералям (3 и 4); б — схема концевых артфии: артерия (1) разделяется на три ветви, не имеющие артериальных соединении, а только капиллярные; закупорка одной ветви (2) лишает соответствующую часть капилляров (3) снабжения кровью (белый инфаркт); в — схема недостаточных коллатералей при геморрагическом инфаркте: Г — артерия, разделяющая на три ветви; Z — просвет средней артерии закупорен; 3 — окольный артериальный сосуд, по которому протекает кровь, заливающая участок, снабжаемый артерией (1), но недостаточный для питания тканей; 4 — вена.
Скорость развития ишемии играет решающую роль: если артериальное малокровие возникает остро, в тканях развиваются дистрофическиеи некротические изменения;если же ишемия носит хронический, медленно прогрессирующий характер, то в ишемизированных органах и тканях нарастают атрофические и склеротические процессы.При этом в тканях обычно успевают сформироваться коллатерали, снижающие степень гипоксии.
Коллатеральное кровообращение иногда приобретает определяющее значение в возможных исходах ишемии. Коллатеральное, или обходное, кровообращение представлено сетью мелких сосудов, соединяющих более крупные артерии и вены. Коллатеральные сосуды имеются в норме, но они находятся в спавшемся состоянии, так как потребности тканей в кровоснабжении обеспечиваются магистральными сосудами. Коллатерали начинают проводить кровь либо в условиях резко возросшей функции органа, либо при возникновении препятствия току крови по магистральному сосуду. В этих случаях раскрываются имеющиеся капилляры и начинают образовываться новые, от скорости их образования зависит уровень компенсации ишемии и ее исход. Однако в некоторых органах, таких как сердце, головной мозг, почки, коллатерали развиты слабо, поэтому при закрытии просвета магистральной артерии коллатеральное кровообращение часто не способно компенсировать ишемию и развивается некроз тканей этих органов. Вместе с тем в подкожной клетчатке, кишечнике и сальнике сеть коллатеральных сосудов в норме развита хорошо, что нередко позволяет этим органам и тканям справиться с ишемией. В остальных органах имеются коллатерали промежуточного типа, которые лишь частично позволяют компенсировать артериальное малокровие (рис. 17).
Значение ишемии заключается в снижении функций ишемизированных органов, которое, однако, может быть обратимым, если ишемия продолжалась относительно недолго и в тканях развились лишь обратимые дистрофические изменения. В случаях медленно нарастающей ишемии в организме успевают развиться компенсаторные иприспособительные процессы, позволяющие в какой-то степени восполнить функцию ишемизированного органа. Если же в ишемизированных органах развиваются некротические изменения с утратой их функций, то это может приводить к тяжелой инвалидности и смерти.
НАРУШЕНИЯ РЕОЛОГИЧЕСКИХ СВОЙСТВ КРОВИ
Эти нарушения проявляются такими патологическими процессами. как тромбоз, эмболия, стаз, сладж. ДВС-синдром.
Тромбоз — процесс прижизненного свертывания крови в просвете сосуда или в полостях сердца.
Свертывание крови является важнейшей физиологической реакцией, препятствующей смертельной потере крови при повреждениях сосудов, и если эта реакция отсутствует, развивается опасное для жизни заболевание — гемофилия. Вместе с тем при повышении свертываемости крови в просвете сосуда образуются свертки крови — тромбы, препятствующие кровотоку, что становится причиной тяжелых патологических процессов в организме, вплоть до наступления смерти. Наиболее часто тромбы развиваются у больных в послеоперационном периоде, у людей, находящихся на длительном постельном режиме, при хронической сердечно-сосудистой недостаточности, сопровождающейся общим венозным застоем, при атеросклерозе, злокачественных опухолях, у беременных, у старых людей.
Причины тромбоза делят на местные и общие:
- Местные причины — повреждение стенки сосуда, начиная от слущивания эндотелия и заканчивая ее разрывом; замедление и нарушения кровотока в виде возникающих завихрений крови при наличии препятствия ее току, например атеросклеротической бляшки, варикозного расширения или аневризмы стенки сосуда.
- Общие причины — нарушение соотношения между свертывающей и противосвертывающей системами крови в результате увеличения концентрации или активности свертывающих факторов — прокоагулянтов (тромбопластинов, тромбина, фибриногена и др.) либо снижения концентрации или активности антикоагулянтов (например, гепарина, фибринолитических веществ), а также повышения вязкости крови, например, всвязи с увеличением количества ее форменных элементов, особенно тромбоцитов и эритроцитов (при некоторых системных заболеваниях крови).
Стадии образования тромба.
Выделяют 4 стадии тромбообразования.
- 1-я — стадия агглютинации тромбоцитов (сосудисто-тромбоцитарная), начинается уже при повреждении эндотелиоцитов интимы и характеризуется адгезией (прилипанием) тромбоцитов к обнаженной базальной мембране сосуда, чему способствует появление определенных факторов свертывания — фибронектина, фактора Виллебрандта и др. Из разрушающихся тромбоцитов выделяется тромбоксан А2 — фактор, суживающий просвет сосуда, замедляющий кровоток и способствующий выбросу тромбоцитами серотонина, гистамина и тромбоцитарного фактора роста. Под влиянием этих факторов запускается каскад свертывающих реакций, в том числе и образование тромбина, который вызывает развитие следующей стадии.
- 2-я — стадия коагуляции (фибриногена (плазменная), характеризуется трансформацией фибриногена в нити фибрина, которые образуют рыхлый сверток и в нем (как в сети) задерживаются форменные элементы и компоненты плазмы крови с развитием последующих стадий.
- 3-я — стадия агглютинации эритроцитов. Она связана с тем, что эритроциты должны передвигаться в потоке крови, а если они останавливаются, то склеиваются (агглютинируют). При этом выделяются факторы, вызывающие ретракцию (сжатие) образовавшегося рыхлого тромба.
- 4-я — стадия преципитации плазменных белков. В результате ретракции из образовавшегося сгустка отжимается жидкость, белки плазмы и белки из распавшихся форменных элементов крови подвергаются преципитации, сверток уплотняется и превращается в тромб, который закрывает дефект стенки сосуда или сердца, но может закрыть и весь просвет сосуда, прекратив тем самым кровоток.
Морфология тромба.
Взависимости от особенностей и скорости образования тромбы могут иметь различный состав, строение и внешний вид. Выделяют следующие виды тромбов:
- белый mpoмб, состоящий из тромбоцитов, фибрина и лейкоцитов, образуется медленно при быстром кровотоке, обычно в артериях, между трабекулами эндокарда, на створках клапанов сердца;
- красный тромб, в состав которого входят эритроциты, тромбоциты и фибрин, возникает быстро в сосудах с медленным током крови, обычно в венах;
- смешанный mpoмб включает в себя тромбоциты, эритроциты, фибрин, лейкоциты и встречается в любых отделах кровеносного русла, в том числе в полостях сердца и в аневризмах артерий;
- гиалиновые тромбы, состоящие из преципитированных белков плазмы и агглютинированных форменных элементов крови, образующих гомогенную, бесструктурную массу; они обычно множественные, формируются тольков сосудах микроциркуляции при шоке, ожоговой болезни, ДВГ-синдроме, тяжелой интоксикации и т. п.
Структура тромба.
Макроскопически в тромбе определяется небольшая, тесно связанная со стенкой сосуда головка тромба, по строению соответствующая белому тромбу, тело — обычно смешанный тромб и рыхло прикрепленный к интиме хвост тромба, как правило, красный тромб. В области хвоста тромб может отрываться, что служит причиной тромбоэмболии.
По отношению к просвету сосуда выделяют:
- пристеночные тромбы, обычно белые или смешанные, не закрывают целиком просвет сосуда, хвост их растет против тока крови;
- обтурирующие тромбы, как правило, красные, полностью закрывающие просвет сосуда, хвост их чаще растет по току крови.
По течению выделяют:
- локализованный (стационарный) тромб, который не увеличивается в размерах и подвергается замещению соединительной тканью — организации
- прогрессирующий тромб, который увеличивается в размерах с различной скоростью, его длина иногда может достигать нескольких десятков сантиметров.
Исходы тромбоза принято подразделять на благоприятные и неблагоприятные.
К благоприятным исходам относят организацию тромба, которая начинается уже на 5-6-й день после его образования и заканчивается замещением тромботических масс соединительной тканью. В ряде случаев организация тромба сопровождается его канализацией,т. е. образованием щелей, через которые в какой-то степени осуществляется кровоток, и васкуляризацией, когда образовавшиеся каналы покрываются эндотелием, превращаясь в сосуды, через которые частично восстанавливается кровоток, обычно через 5-6 нед после тромбоза. Возможно обызвествление тромбов (образование флеболипов).
Неблагоприятные исходы: тромбоэмболия, возникающая при отрыве тромба или его части, и септическое (гнойное) расплавление тромба при попадании в тромботические массы гноеродных бактерий.
Значение тромбоза определяется быстротой образования тромба, его локализацией и степенью сужения сосуда. Так, мелкие тромбы в венах малого таза сами по себе не вызывают каких-либо патологических изменений в тканях, но, оторвавшись, могут превратиться в тромбоэмболы. Пристеночные тромбы, незначительно суживающие просветы даже крупных сосудов, могут не нарушать в них гемодинамику и способствовать развитию коллатерального кровообращения. Обтурирующие тромбы артерий являются причиной ишемии,заканчивающейся инфарктом или гангреной органов. Тромбоз вен (флеботромбоз) нижних конечностей способствует развитию трофических язв голеней, кроме того, тромбы могут стать источником эмболии. Шаровидный тромб, образующийся при отрыве от эндокарда левого предсердия, периодически закрывая атриовентрикулярное отверстие, нарушает центральную гемодинамику, в связи с чем больной теряет сознание. Прогрессирующие септические тромбы, подвергающиеся гнойному расплавлению, могут способствовать генерализации гнойного процесса.
Эмболия — циркуляция в крови или лимфе не встречающихся в норме частиц (эмболов) и закупорка ими просвета сосудов (рис. 18).
По происхождению выделяют экзо- и эндогенные эмболии.
При экзогенных эмболиях эмболы попадают в сосудистое руло из окружающей среды. Различают воздушную, газовую эмболию и эмболию инородными телами.
Воздушная эмболия происходит при попадании воздуха через поврежденные крупные вены шеи (имеющие отрицательное давление по отношению к атмосферному), через зияющие после отторжения плаценты вены матки, при введении воздуха с лекарственными препаратами с помощью шприца или капельницы, при пневмотораксе (попадании воздуха в плевральные полости). Воздушные эмболы обтурируют капилляры легких, головного мозга; воздушные пузыри, скапливающиеся в правых отделах сердца, придают имеющейся в них крови пенистый вид.
Газовая эмболия развивается при быстрой декомпрессии (у водолазов при быстром подъеме с глубины, при разгерметизации кабины самолета, барокамеры), приводящей к высвобождению из крови азота. Газовые эмболы поражают различные органы, в том числе головной и спинной мозг, вызывая кессонную болезнь.
Эмболия инородными телами возникает при попадании в травмированные крупные сосуды частиц инородных предметов — медицинских катетеров, осколков ампул, кусочков одежды или осколков пуль и снарядов при огнестрельных ранениях.
При эндогенных эмболиях эмболами являются собственные ткани организма: тромбоэмболия, жировая, тканевая и микробная эмболия.
Тромбоэмболия развивается при отрыве тромба или его части и является наиболее частой эмболией. Ее источником могут быть тромбы любой локализации — артерий, вен. полостей и створок клапанов сердца. Самой распространенной является тромбоэмболия легочной артерии, возникающая обычно у больных в послеоперационном периоде, при варикозном расширении вен нижних конечностей, тромбофлебите или флеботромбозе у больных, страдающих сердечно-сосудистой недостаточностью, онкологическими заболеваниями.
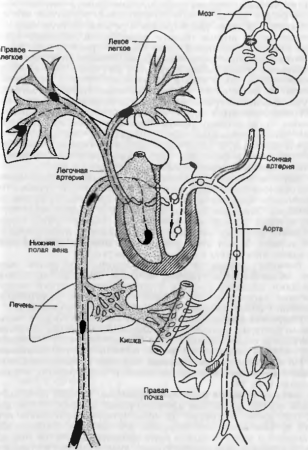
Рис. 18. Схема направления движения эмболов (по Я. Л. Рапопорту). Из венозной системы эмболы заносятся в правую половину сердца, а оттуда в легочный ствол и легкие (область распространения эмболов из венозной сети заштрихована). Из левых отделов сердца эмболы заносятся по артериям в разные органы (указано стрелками).
При этом тромбоэмболы попадают в легочный ствол илилегочные артерии из вен нижних конечностей, жировой клетчатки малого таза, иногда из печеночных вен, нижней и верхней полых вен илиправых отделов сердца с пристеночными тромбами, что, как правило, заканчивается смертью. Механизм смерти связан с пульмоно-коронарным рефлексом который возникает при ударе тромбоэмбола в рефлексогенную зону, расположенную в интиме области разветвления легочного ствола. При этом остро возникает спазм сосудов сердца, легких, а также бронхов и наступает остановка сердца. Определенную роль играет и закрытие тромбоэмболом просвета легочного ствола. Мелкие тромбоэмболы могут проходить легочный ствол и обтурировать мелкие ветви легочной артерии, вызывая инфаркты легких. В случае массивной тромбоэмболии мелких ветвей легочных артерий может развиться острое падение артериального давления — коллапс. Оторвавшиеся тромбы створок клапанов или пристеночные тромбы эндокарда, образующиеся при эндокардитах, инфаркте миокарда, в хронической аневризме сердца, с током крови попадают по большому кругу кровообращения в различные органы, вызывая тромбоэмболический синдром.
Жировая эмболия возникает при переломах трубчатых костей, размозжении подкожной жировой клетчатки при травмах, при ошибочном введении в кровяное русло масляных лекарственных растворов. Жировые эмболы закупоривают мелкие ветви легочных артерий, причем если обтурировано больше 2/3 этих сосудов, то может развиться острая правожелудочковая недостаточность, что, однако, бывает очень редко. Чаще жировая эмболия легких вызывает пневмонию в пораженных участках.
Тканевая эмболия является результатом разрушения тканей при заболеваниях и травмах, например эмболия опухолевыми клетками, лежащая в основе формирования метастазов опухоли, эмболия околоплодными водами у родильниц, разрушенными тканями у новорожденных с тяжелыми родовыми травмами.
Микробная эмолия возникает при закупорке сосудов скоплениями бактерий, грибов, простейшими и животными паразитами (например, альвеококками). Этот вид эмболии, чаще наблюдается при гнойном расплавлении тромба, особенно при септикопиемии.
По механизму распространения выделяют эмболии большого ималого круга кровообращения, орто- и ретроградную, парадоксальную (рис. 18).
Эмболии большого круга кровообращения— эмбол из левых отделов сердца, аорты или других крупных артерий, перемещаясь по току крови, обтурирует органные артерии, в результате чего в этих органах возникают инфаркты или гангрена. Эмболы, образующиеся в венах большого круга кровообращения, по току крови обтурируют либо воротную вену, либо попадают в правые отделы сердца и оттуда — в малый круг кровообращения.
При эмболии малого круга кровообращения эмбол из правых отделов сердца проходит в малый круг кровообращения, вызывая либо эмболию легочного ствола, ведущую к остановке сердца, либо инфаркты легких.
При ортоградной эмболии эмбол перемещается по току крови или лимфы — наиболее частый вид эмболии.
Ретроградная эмболт характеризуется движением эмбола против тока или лимфы и возникает обычно при эмболии тяжелыми инородными телами или при ретроградном лимфогенном метастазировании рака желудка.
Парадоксальная эмболия развивается при проникновении эмбола из венозного отдела большого круга кровообращения в артериальный отдел, минуя легкие. Это редкий вид эмболии, которая наблюдается при незаращении межжелудочковой или межпредсердной перегородки в сердце (например, при незаращении овального окна), при артериовенозных анастомозах, прежде всего при открытом артериальном (боталловом) протоке или при травматическом образовании артериовенозного соустья.
Значение эмболии определяется ее видом, распространенностью и локализацией. Особенно опасны эмболии головного мозга, сердца, легочного ствола, часто заканчивающиеся смертью больного, тогда как поражение почек, печени, селезенки, скелетных мышц имеет меньшее значение. Однако в любом случае эмболия кровеносных сосудов приводит к нарушению кровообращения в тканях, вызывает их ишемию и некроз. Эмболия лимфатических сосудов, особенно нижних конечностей, может приводить к лимфатическому отеку тканей, их склерозу и снижению функции органа, например значительное увеличение размеров нижней конечности при слоновости.
НАРУШЕНИЯ МИКРОЦИРКУЛЯЦИИ
Причины расстройств микроциркуляции:
- нарушения центрального и регионарного кровообращения —
- развиваются при сердечной недостаточности, артериальной и венозной гиперемии, при ишемии;
- изменения вязкости и объема крови (лимфы) — наблюдаются при уменьшении объема жидкости в плазме (гипогидратация), увеличении количества форменных элементов (полицитемия) или белков плазмы, агрегации и агглютинации клеток крови;
- гемодилюция, или разжижение крови, — возникает в результате значительного поступления тканевой жидкости в кровь (гипергидратация), снижения общего числа форменных элементов крови (панцитопения), уменьшения содержания белков плазмы (гипопротеинемия).
По локализации первично возникающих нарушений расстройства микроциркуляции разделяют на внутрисосудистые, трансмуральные ивнесосудистые.
Внутрисосудистые нарушения ликроциркуляции проявляются следующим образом:
- замедление, вплоть до прекращения (стаза), тока крови или лимфы наиболее часто возникает при сердечной недостаточности, ишемии, венозной гиперемии, сгущении крови (при профузном поносе, неукротимой рвоте, ожоговой болезни и т. п.):
- чрезмерное ускорение кровотока наблюдается при артерио-ловенулярных шунтах, гемодилюции, почечной недостаточности;
- нарушение ламинарности (турбулентность) тока крови или лимфы возникает при образовании препятствия микроциркуляции в виде образования агрегатов из клеток крови (при по-лицитемии), формировании микротромбов, атипичном строении микрососудистого русла (капиллярная гемангиома).
Транс муральные нарушения микроциркуляции связаны с изменениями в самой стенке микрососудов, через которую в норме проходит плазма крови и ее форменные элементы, поступают продукты метаболизма и регулирующие обмен веществ биологически активные вещества. В патологии наиболее существенную роль играют две группы нарушений трансмуральной микроциркуляции:
- изменение объема транспорта плазмы (лимфы), который может возрастать (при артериальной гиперемии, аллергических реакциях, лимфостазе) или уменьшаться (при спазме артериол, кальцификации стенок микрососудов);
- увеличение транспорта клеток крови через стенки микрососудов, что может быть при значительном повышении их проницаемости (например, при гипоксии) или при нарушении целостности (эритроцитов).
Внесосудистые нарушения микроциркуляции заключаются в замедлении вплоть до прекращения тока межклеточной жидкости и обусловлены изменениями влияний на микроциркуляцию внесосудистых факторов, например нервно-трофической регуляции метаболизма, появлением в окружающих тканях медиаторов воспаления (гистамин, серотонин и др.), которые резко усиливают микровезикулярный транспорт, но могут и способствовать тромбированию сосудов микроциркуляции; при скоплении в интерстициальной ткани жидкости, например, транссудата при отеках или экссудата при воспалении, повышается давление тканевой жидкости и она сдавливает сосуды микроциркуляции.
НАРУШЕНИЯ МИКРОЦИРКУЛЯЦИИ
Нарушения микроциркуляции, имеющие нередко самостоятельное клиническое значение и возникающие при многих заболеваниях, — сладж-феномен, стаз, ДВС-синдром.
СЛАДЖ-ФЕНОМЕН
Сладж-феномен (от англ. sludge — тина, густая грязь) характеризуется адгезией и агрегацией форменных элементов крови, прежде всего эритроцитов, что вызывает значительные гемодинамические нарушения. Клетки в состоянии сладжа имеют вид «монетных столбиков», сохраняя при этом свои цитомембраны (рис. 19).
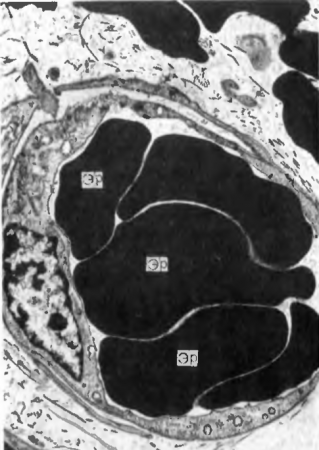
Рис. 19. Агрегация эритроцитов как проявление сладж-феномена. В просвете капилляра несклеиваюшиеся эритроциты (Эр) в виде монетного столбика.
Причишит сладжа являются нарушения центральной и регионарной гемодинамики, повышение вязкости крови и повреждение стенок микрососудов (см. выше). В основе сладж-феномена лежат следующие механизмы:
- активация клеток крови и выделение ими веществ, способствующих агрегации эритроцитов. — АДФ. тромбоксана А2. кининов, гистамина, простагландинов и др.;
- смена поверхностного заряда клеток крови с отрицательного на положительный в результате избытка катионов, поступающих из поврежденных клеток;
- уменьшение величины поверхностного заряда мембран клеток крови при избытке макромолекул белка (гиперпротеинемии), особенно за счет увеличения концентрации иммуноглобулинов, фибриногена, аномальных белков.
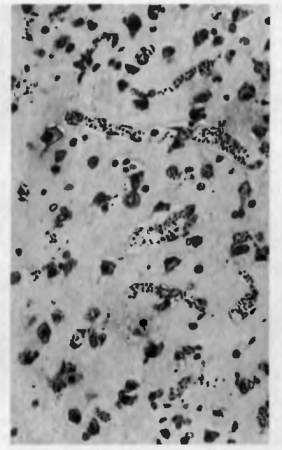
Рис. 20. Стаз в капиллярах мозга (при малярии). Капилляры резко расширены, в их просветах склеившиеся эритроциты и пигмент гемомеланин. Ткань мозга отечна.
Последствия сладжа
- замедление кровотока в микроциркуляторном русле, вплоть до его остановки;
- нарушения транскапиллярного обмена;
- гипоксия, ацидоз и нарушение метаболизма окружающих тканей.
Значение сладжа.
Изменения, сопровождающие сладж-феномен, приводят к повышению проницаемости стенок капилляров и венул, пропитыванию их плазмой крови (плазморрагия), отеку и нарастающей ишемии окружающих тканей. В целом, совокупность указанных изменений обозначается как синдром капилляро-трофической недостаточности. Сладж может быть обратимым, и тогда постепенно восстанавливается микроциркуляция, но сладж может предшествовать полной остановке крови (стазу), а также агглютинации и распаду форменных элементов крови в «монетных столбиках» с образованием в капиллярах гиалиновых тромбов.
СТАЗ
Стаз — остановка кровотока в сосудах микроциркуляторного русла, прежде всего в капиллярах, реже — в венулах (рис. 20). Остановке крови предшествует ее замедление — престаз,вплоть до развития сладж-феномена.
Причинами стаза являются инфекции, интоксикации, шок, длительное искусственное кровообращение, воздействие физических, в том числе температурных, факторов (например, «холодовый стаз» при отморожениях).
Механизмы стаза во многом схожи с механизмами сладж-феномена:
- утрата эритроцитами способности находиться во взвешенном состоянии и образование их агрегатов, что затрудняет ток крови по микрососудам и вызывает остановку кровотока в капиллярах:
- изменения реологических свойств крови, аналогичных тем, которые возникают при сладж-феномене;
- гипоксия, ацидоз, нарушения и прекращение метаболизма;
- дистрофические или некротические изменения окружающих тканей в зависимости от длительности стаза крови.
Исход стаза. После устранения причины, вызвавшей стаз, кровоток в сосудах микроциркуляторного русла может восстановиться. а в окружающих тканях какое-то время сохраняются дистрофические изменения, которые, однако, в этих условиях также обратимы. Если же стаз капилляров устойчив, то гипоксия в окружающих тканях приводит к их некрозу.
Значение стаза определяется его локализацией и продолжительностью. Острый стаз в большинстве случаев приводит к обратимым изменениям в тканях, но в головном мозге он может способствовать развитию тяжелого, иногда смертельного отека ткани мозга с дислокацией его стволовой части в большое затылочное отверстие, что наблюдается, например, при коме. В случаях длительного стаза возникают множественные микронекрозы и иные кровоизлияния.
СИНДРОМ ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ КРОВИ (ДВС-СИНДРОМ)
Синдром диссеминированного внутрисосудистого свертывания крови (ДВС-синдром) характеризуется образованием множественных тромбов в сосудах микроциркуляторного русла различных органов и тканей вследствие активации факторов свертывания крови и развивающимся в связи с этим их дефицитом, что приводит к усилению фибринолиза. падению свертываемости крови и многочисленным кровоизлияниям. ДВС-синдром часто развивается при шоке любого происхождения (травматическом, анафилактическом, геморрагическом, кардиальном и др.), при переливании несовместимой крови, злокачественных опухолях, после хирургических вмешательств, при тяжелой интоксикации и инфекции, в акушерской патологии, при трансплантации органов, использовании аппаратов искусственной почки и искусственного кровообращения и др.
В своем развитии ДВС-синдром проходит 4 стадии.
- 1-я стадия — гиперкоагуляции и тромбообразования — характеризуется внутрисосудистой агрегацией форменных элементов, диссеминированным (т. е. во многих микрососудах одновременно) свертыванием крови и формированием множественных тромбов в микрососудах разных органов и тканей. Эта стадия длится всего 8—10 мин.
- 2-я стадия — нарастающая коагулопатия потребления, особенностью которой является значительное снижение числа тромбоцитов и уровня фибриногена, израсходованных на образование тромбов в предыдущей стадии. Поэтому свертываемость крови снижается и в результате развивается геморрагический диатез, т. е. множественные мелкие кровоизлияния.
- 3-я стадия — глубокой гипокоагуляции и активации фибринолиза, которая наступает через 2—8 ч от начала ДВС-синдрома. Название стадии говорит о том, что в этом периоде практически прекращаются процессы свертывания крови вследствие истощения всех свертывающих факторов и одновременно резко активизируются процессы фибринолиза (т. е. растворения фибрина, тромбов). Поэтому возникает полная несвертываемость крови, развиваются кровотечения и множественные кровоизлияния.
- 4-я стадия — восстановительная, или остаточных проявлений, заключается в дистрофических, некротических и геморрагических изменениях тканей многих органов. При этом примерно в 50 % случаев может наступить полиорганная недостаточность (почечная, печеночная, надпочечниковая, легочная, сердечная), приводящая больных к смерти. При благоприятном исходе заболевания наступает восстановление поврежденных тканей и восстанавливаются функции органов.
В зависимости от распространенности выделяют варианты ДВС-синдрома: генерализованный и местный.
В зависимости от продолжительности ДВС-синдрома выделяют следующие формы:
- острую (от нескольких часов до нескольких суток), протекающую наиболее тяжело, развивается при шоке, характеризуется генерализованным некротическим и геморрагическим поражением органов с развитием полиорганной недостаточности;
- подострую (от нескольких дней до недели), развивается чаще при поздних гестозах, лейкозах, злокачественных опухолях. характеризуется локальными или мозаичными тромбогеморрагическими повреждениями тканей;
- хроническую (несколько недель и даже месяцев), которая чаще развивается при аутоиммунных заболеваниях, длительной интоксикации, при злокачественных опухолях: у больных отмечаются обычно локальные или мигрирующие изменения в органах с развитием их медленно прогрессирующей недостаточности.
Патологическая анатомия ДВС-синдрома заключается в образовании в капиллярах и венулах множественных микротромбов, как правило, состоящих из фибрина, стаза в капиллярах, кровоизлияний, дистрофических и некротических изменений в различных органах.
НАРУШЕНИЯ ПРОНИЦАЕМОСТИ СТЕНОК СОСУДОВ
При повреждении стенок сосудов или полостей сердца, а также при повышении сосудистой проницаемости вытекает содержащаяся в сосудах или в сердце кровь. Исходя из особенностей и последствий кровопотери выделяют кровотечение и кровоизлияние.
Кровотечение (haemorrhagia) — выход крови за пределы сосудистого русла или сердца в окружающую среду (наружное кровотечение), а также в полости тела или в просвет полого органа (внутреннее кровотечение). Примером наружного кровотечения являются кровотечение из полости матки (метроррагия), из кишечника (мелена), кровотечения при травмах конечностей или тканей поверхности тела. Внутренними являются кровотечения в полость перикарда (гемоперикард), в полости грудной клетки (гемоторакс), в брюшную полость (гемоперитонеум).
По источнику кровотечения выделяют:
- артериальное;
- венозное;
- артериально-венозное (смешанное);
- капиллярное;
- паренхиматозное кровотечение (капиллярное из паренхиматозных органов);
- сердечное кровотечение.
Кровоизлияние — частный вид кровотечения, при котором вышедшая из сосудов кровь накапливается в окружающих тканях. Выделяют 4 разновидности кровоизлияния:
- гематома — кровоизлияние, при котором в тканях образуется полость, заполненная кровью;
- кровоподтек — плоское кровоизлияние в коже, подкожной клетчатке, слизистых оболочках;
- геморрагическое пропитывание (имбибиция) — диффузное кровоизлияние без четких границ;
- петехии — точечные кровоизлияния в коже, слизистых и серозных оболочках и под капсулами внутренних органов.
Механизмы развития кровотечений и кровоизлияний:
- разрыв сосуда или стенки сердца (haemorrhagia per rexin) при травме, некрозе (инфаркте), аневризме;
- разъедание стенки сосуда (haemorrhagia per diabrosin), что происходит при воспалении ткани или при злокачественном росте, например в дне язвы желудка или в опухоли, при прорастании ворсинами хориона сосудов маточной трубы при внематочной беременности и др.;
- диапедез (haemorrhagia per diapedesin, от греч. dia — через, pedao — скачу) характеризуется выходом крови из сосуда в результате повышения проницаемости его стенки без нарушения ее целостности. Это один из наиболее частых механизмов кровоизлияния наблюдается при гипоксии, интоксикациях, инфекциях, различных коагулопатиях, геморрагических диатезах, при гипертоническом кризе, гемофилии и др. (рис. 21).
Исход кровоизлияния может быть благоприятным когда излившаяся кровь рассасывается, как, например, при кровоподтеке, или организовывается, что бывает при гематомах, но может быть и неблагоприятным, если кровоизлияние происходит в жизненно важные органы — головной мозг, надпочечники. В этом случае больной может погибнуть или становится инвалидом.
Значение кровотечения обусловлено его видом, выраженностью и продолжительностью. Так, больной может погибнуть при небольшом кровоизлиянии в область ствола головного мозга и при острой массивной артериальной кровопотере. Вместе с тем повторяющиеся в течение длительного времени, но небольшие кровотечения, например при геморрое или из язвы желудка, обусловливают лишь развитие постгеморрагической анемии, сопровождающейся жировой дистрофией паренхиматозных органов. Большое значение имеет скорость кровотечения — быстрая кровопотеря даже относительно небольших объемов крови (300— 350 мл) приводит больного к смерти, в то время как потеря значительно больших объемов крови, но на протяжении длительного времени (маточные или геморроидальные кровотечения) не вызывает тяжелых осложнений, так как в организме успевают развиться компенсаторные процессы.
НАРУШЕНИЯ ЛИМФООБРАЩЕНИЯ
Патологические изменения функций лимфатической системы тесно связаны с нарушениями кровообращения и усугубляют возникающие при этом изменения в тканях. Среди нарушений лимфообращения основную роль играют лимфатическая недостаточность и лимфостаз.
ЛИМФАТИЧЕСКАЯ НЕДОСТАТОЧНОСТЬ
Лимфатическая недостаточность — состояние при котором интенсивность образования лимфы превышает способность лимфатических сосудов транспортировать ее в венозную систему. Выделяют следующие виды недостаточности лимфатической системы: механическую, динамическую и резорбционную.
При механической недостаточности возникает органическое или функциональное препятствие току лимфы, что происходит при закупорке лимфатических сосудов опухолевыми клетками, сидерофагами, сдавлении лимфатических путей опухолью, а также при венозном застое.
Динамическая недостаточность наблюдается при несоответствии между количеством тканевой жидкости и возможностями лимфатических путей для ее отведения, что имеет место при значительном повышении проницаемости кровеносных сосудов в связи с воспалением, аллергическими реакциями, при выраженных отеках тканей.
Резорбционная недостаточность обусловлена уменьшением проницаемости стенок лимфатических капилляров или изменением дисперсных свойств тканевых белков.
Лимфостаз — остановка тока лимфы, что происходит при недостаточности лимфатической системы вне зависимости от механизма ее развития. Выделяют общий и регионарный лимфостаз.
Общий лимфостаз возникает при общем венозном застое, так как при этом уменьшается перепад давления между кровью и лимфой — один из главных факторов, определяющих отток лимфы из лимфатических сосудов в венозную систему.
Регионарный лимфостаз развивается при местной венозной гиперемии, при закупорке регионарных лимфатических сосудов или при сдавлении их опухолью.
Последствием лимфостаза является лимфатический отек — лимфедема. Длительный застой лимфы способствует активации фибробластов и разрастанию соединительной ткани, что приводит к склерозу органов. Лимфатический отек и склероз тканей вызывают стойкое увеличение объема органа либо той или иной части тела — нижних конечностей, половых органов и др., и развивается заболевание, которое называется слоновостью.