ОБЩАЯ ХАРАКТЕРИСТИКА ИММУННОЙ СИСТЕМЫ
Иммуногенная реактивность — ответ организма на антигенный стимул. Материальным субстратом иммуногенной реактивности является иммунная, или иммунокомпетентная, система (ИКС). Иммунная система представляет собой совокупность органов, тканей и клеток, обеспечивающих биохимическую, структурную и функциональную однородность и индивидуальность организма путем обнаружения, уничтожения и удаления (элиминации) из него чужеродных антигенов.
Эволюционно иммунная система сформировалась как механизм контроля за однородным и индивидуальным антигенным составом организма. В основе этого механизма лежит способность клеток иммунной системы отличать собственные клетки и белковые соединения от чужеродных. Обнаружение последних сопровождается инактивацией, разрушением и элиминацией их из организма.
Антиген — вещество экзо- или эндогенного происхождения, вызывающее иммунную реакцию, которая заключается в выработке иммунных антител и лимфоцитов, их взаимодействии с антигеном, сопровождающимся его инактивацией и элиминацией.
Виды антигенов.
Антигены разделяют на несколько групп в зависимости от их биохимической структуры, происхождения, пути попадания в организм и других критериев.
По биохимической структуре антигены делят на два вида:
- белки и белоксодержащие соединения;
- небелковые соединения — гаптены, к которым относятся полисахариды, липиды, некоторые синтетические полимеры, неорганические вещества (соединения йода, брома, висмута), лекарственные средства.
Сами по себе гаптены неиммуногенны. Однако после их соединения с белками или клетками организма они приобретают способность вызывать иммунные реакции.
По происхождению антигены делят на экзо- и эндогенные.
Экзогенные антигены составляют большую часть антигенов:
- инфекционно-паразитарного происхождения (антигены вирусов, риккетсий, бактерий, паразитов);
- неинфекционного происхождения (чужеродные белки и белоксодержащие соединения, гаптены, входящие в состав пыли, пищевых продуктов, пыльцы растений, ряда лекарственных веществ).
Эндогенные антигены также подразделяют на:
- инфекционные и/или паразитарные (белковые компоненты микробов, «заселяющих» миндалины, кишечник, слизистые оболочки рта, дыхательных путей);
- неинфекционные, которые образуются при повреждении собственных белков, при конъюгации гаптенов с белками клеток и биологических жидкостей организма, при мутациях в геноме клеток или при выработке ими аномальных белков.
Иммунная система представлена тремя субсистемами клеток: А, В и Т.
Субсистему А-клеток составляют мононуклеарные клетки — моноциты, тканевые макрофаги и некоторые другие. Эти клетки обладают высокой способностью обнаруживать чужеродные антигены. поглощать их. выявлять их молекулярную структуру, передавать информацию о них Т- и В-лимфоцитам.
Субсистема В-клеток состоит из различных клонов В-лимфоцитов. При первом контакте антигена с В-лимфоцитами часть их превращается в плазматические, антителопродуцирующие клетки. а часть — в долгоживущие, рециркулирующие клетки иммунной памяти. Повторный контакт этих клеток с тем же антигеном сопровождается массированной бласттрансформацией лимфоцитов памяти и трансформацией их в плазматические клетки, вырабатывающие специфические иммуноглобулины — антитела. У человека выделяют 5 основных классов иммуноглобулинов: А, Е, G, М, D.
Субсистема Т-клеток представлена различными клонами Т-лимфоцитов. Их пролиферация и созревание происходят в основном с участием вилочковой железы (тимуса), с чем связано их обозначение: Т-лимфоциты, т. е. тимусзависимые. Первый контакт Т-клеток с антигеном сопровождается их дифференцировкой в зрелые, долгоживущие лимфоциты различных субполяций. включая клетки памяти. При повторном контакте с тем же антигеном клетки памяти превращаются в специфические Т-лимфоциты различных клонов.
В субсистемах Т- и В-лимфоцитов имеются «исполнительные» клетки:
- плазматические, продуцирующие иммуноглобулины;
- Тл — киллеры (убийцы), разрушающие клетки и ткани, несущие чужеродный антиген;
- Тл-хелперы, т. е. помощники;
- Тл-супрессоры, т. е. сдерживающие. Они влияют на пролиферацию и дифференцировку других лимфоцитов.
Иммунный ответ организуется клетками всех субсистем ИКС,
сопровождается развитием разнообразных иммунопатологических состояний, реализующихся через воспаление. Инициальным этапом иммунной реакции является распознавание антигена: если он чужероден для организма, информация о нем передается эфферентным клеткам ИКС.
ТИПОВЫЕ ФОРМЫ ИММУНОПАТОЛОГИЧЕСКИХ ПРОЦЕССОВ
Иммунопатологические процессы — это реакции организма, развивающиеся в результате нарушений иммунитета. В большинстве случаев они являются следствием дефекта или истощения одного или нескольких механизмов, необходимых для обеспечения эффективного иммунного ответа.
ВИДЫ ИММУНОПАТОЛОГИЧЕСКИХ ПРОЦЕССОВ
По происхождению:
Первичные (наследственные, врожденные). Они являются результатом генетического дефекта, обусловливающего нарушения процессов пролиферации, дифференцировки и функционирования клеток А-, В- или Т-лимфоцитов иммунной системы.
Вторичные (приобретенные в постнатальном периоде онтогенеза). Развиваются под влиянием повреждающих факторов физического характера (например, высокой дозы рентгеновского излучения), химического (например, действия цитостатических агентов) или биологического (например, значительного повышения уровня в крови глюкокортикоидов, повреждения клеток иммунной системы при вирусной или бактериальной инфекции).
По механизмам развития:
- Обусловленные отсутствием или значительным уменьшением количества А-клеток, различных популяций В- или Т-лимфоцитов, в связи с подавлением процессов их деления, созревания или в связи с усиленным разрушением.
- Обусловленные нарушением дифференцировки, макрофагов, Т- и В-лимфоцитов, а также их кооперации в результате изменения количества в организме Т- и В-лимфоцитов регуляторов (увеличение числа «супрессоров», уменьшение «хелперов») или биологически активных веществ (кортикостероидов. интерлейкинов, гормонов и др.).
По преимущественному повреждению клеток различных иммунных субсистем:
- «В-зависимые»(«гуморальные»);
- «Т-зависимые» («клеточные»):
- «A-зависимые» («фагоцитарные», «мононуклеарные»).
- Комбинированные.
Характеристика отдельных иммунопатологических процессов
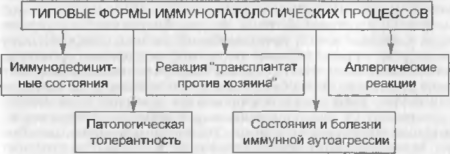
Выделяют несколько основных групп типовых расстройств иммунитета: иммунодефицитные состояния (ИДС), патологическую толерантность, реакцию «трансплантат против хозяина», аллергические реакции, состояния иммунной аутоагрессии (схема 2).
Иммунодефицитные состояния
Иммунодефицитные состояния (или иммунодефициты) характеризуются значительным снижением активности или неспособностью организма к эффективному осуществлению реакций клеточного или гуморального иммунитета. Они проявляются высокой склонностью организма к развитию инфекционных, паразитарных, опухолевых и аллергических заболеваний.
Главным звеном патогенеза иммунодефицитов является блокада процессов деления и/или созревания клеток А-, Т- или В-субсистем ИКС либо деления и дифференцировки их клеток-предшественников.
Примером иммунодефицитного состояния может служить синдром ретикулярной дискинезии. Она характеризуется значительным уменьшением в костном мозге количества стволовых гемопоэтических клеток и блокадой созревания из них лимфо- и моноцитов с развитием дефицита клеток А-, В- и Т-субсистем. Пациенты, страдающие этим синдромом, погибают вскоре после рождения от различных инфекций или злокачественных опухолей.
Схема 2
Нарушения в субсистеме А-клеток проявляются расстройством фагоцитоза, процессов «переработки» и представления антигена лимфоцитам.
Расстройства деления и созревания В- или Т-лимфоцитов обусловливают нарушение реакций гуморального и клеточного иммунитета. В связи с этим у больных часто наблюдаются вирусные, бактериальные и грибковые инфекции, заболеваемость новообразованиями увеличивается более чем в 100 раз.
Виды иммунодефицитных состояний
Синдром приобретенного иммунодефицита (СПИД) является одним из наиболее ярких иммунодефицитных состояний. Впервые описан в научной литературе в 1981 г. Однако ретроспективный анализ свидетельствует о том, что СПИД поражал людей и ранее. Первые случаи синдрома были зарегистрированы в США, Африке, на Гаити. В последние годы установлено, что каждые 12—14 мес число зарегистрированных случаев заболевания удваивается. Наибольшее распространение СПИД имеет среди гомо- и бисексуальных мужчин; наркоманов, вводящих наркотики внутривенно и пользующихся «коллективными» шприцами; реципиентов гемотрансфузий (больные анемиями); детей, родители которых больны СПИДом.
Возбудителем СПИДа является вирус, который обозначают как ВИЧ — вирус иммунодефицита человека или ЛАВ — лимфаденопатический вирус. Он относится к группе ретровирусов подсемейства лентивирусов. Ретровирусы содержат однонитчатую линейную РНК и фермент ревертазу. Репликация вирусной нуклеиновой кислоты идет через стадию синтеза двунитчатой ДНК на матрице РНК, т. е. как бы обратным путем (отсюда название фермента — ревертаза и группы вирусов — ретровирусы).
Попав в организм, возбудитель СПИДа внедряется в клетки, содержащие рецептор Т4, к которому вирусы высокоспецифичны. Наиболее богаты такими рецепторами Т-лимфоциты-хелперы. Однако, помимо этих клеток, вирус способен внедряться также и в моноциты, тканевые макрофаги, клетки глии, нейроны. В ядро клетки-мишени проникает ДНК-копия с РНК вируса, которая внедряется в клеточный геном. Вирус обнаруживается в крови, в ткани слюнных желез, предстательной железы, яичек. Через 6— 8 нед (реже через 8—9 мес) после инфицирования организма в крови появляются антитела к ВИЧ. С этого момента инфицирование организма может быть выявлено современными методами.
Действие ВИЧ на клетки организма приводит к их лизису и уменьшению их числа. В наибольшей мере это относится к Т-лимфоцитам-хелперам. Именно поэтому развивается лимфопения. Одновременно примерно на 80—90 % снижаются количество и функциональная активность Т-лимфоцитов-киллеров. Число В-лимфоцитов, как правило, остается в пределах нормы, но функциональная активность их снижена.
Количество макрофагов и других А-клеток не изменяется, однако нарушаются хемотаксис и внутриклеточное переваривание чужеродных агентов. Нарушается также механизм представления макрофагом антигена Т- и В-лимфоцитам. Эти изменения создают предрасположенность больных СПИДом к инфекциям, лимфоретикулярным опухолям — к саркоме Капоши.
В лимфатических узлах больных СПИДом выявляется гиперплазия фолликулов, в основном за счет увеличения количества Т-супрессоров. С одержание Т-хелперов значительно снижено. В тимусе обнаруживается атрофия эпителиальных и уменьшение числа лимфоидных клеток. Таким образом, СПИД представляет собой вариант комбинированного иммунодефицитного состояния.
Толерантность
Толерантность (от лат. tolerantia — переносимость, терпимость) — состояние, характеризующееся «терпимостью», т. е. отсутствием реакции иммунной системы на чужеродные антигены. При этом состоянии в иммунной системе нарушена выработка иммунных лимфоцитов, либо клетки иммунной системы не вырабатывают антител, либо не реализуется эфферентное звено иммунитета — уничтожение и элиминация носителя чужеродной антигенной информации.
Толерантность может быть подразделена на три разновидности: физиологическую, патологическую и индуцированную.
Основные механизмы патологической толерантности:
- отсутствие, недостаточное количество или нарушение функции клеток иммунной системы, т. е. имтнодефицитное состояние;
Физиологическая толерантность — терпимость иммунной системы антигенов собственных белков организма. При этом те клоны иммунных клеток, которые в период эмбрионального развития подвергаются массированному воздействию антигенов собственных белков, гибнут и выводятся из организма.
Одной из форм физиологической толерантности является изоляционная толерантность. Она распространяется на антигены клеток тканей, изолированных от иммунокомпетентной системы структурно-физиологическими барьерами. К ним относятся ткань головного мозга, хрусталик глаза, яички, щитовидная железа.
Патологическая толерантность. В этом случае речь идет о «терпимости» иммунной системой чужеродных антигенов, чаще всего бактерий, вирусов, многоклеточных паразитов, клеток злокачественных опухолей или трансплантата.
- повышение активности Т- и В-лимфоцитов-супрессоров, которые тормозят созревание «эффекторных» клеток иммунной системы — Т-лимфоцитов-киллеров и плазматических клеток;
- угнетение или блокада реакций клеточного иммунитета на антиген.
Это происходит тогда, когда специфические иммуноглобулины, взаимодействуя с антигенами клеток не способны инактивировать их. Антигенные детерминанты клеток закрываются («экранируются») этими «недееспособными» антителами или комплексами «антиген—антитело». Т-лимфоциты-киллеры в таком случае не способны обнаружить «экранированную» чужеродную клетку.
Индуцированная толерантность (искусственная, лечебная) достигается с помощью воздействий, целенаправленно подавляющих активность иммунных клеток, таких как ионизирующее излучение, высокие дозы цитостатиков, иммунодепрессанты. Они вызывают лизис, торможение или блокаду деления и созревания клеток иммунной системы. Индуцированную толерантность в медицине используют с целью повышения успеха трансплантации органов и тканей, лечения аллергических реакций.
Реакция «трансплантантат против хозяина» (РТПХ)
Реакция развивается в случае трансплантации реципиенту большой массы тканей донора, содержащих иммунные клетки (например, костного мозга или лейкоцитной массы). Течение РТПХ усугубляется при пониженной активности иммунной системы «хозяина» (например, при воздействии ионизирующего излучения. иммунодепрессантов). РТПХ характеризуется поражением органов и тканей иммунокомпетентной системы реципиента, а также повреждением кожи, желудочно-кишечного тракта (особенно в зоне расположения групповых лимфатических фолликулов — пейеровых бляшек), печени.
Клинико-морфологические проявления РТПХ заключаютсяв развитии некротических и дистрофических поражений указанных органов, лимфопении, анемии, тромбоцитопении, диспепсических расстройств (тошнота, рвота, диарея), увеличении печени. У взрослых описанное состояние обозначают термином «гомологическая болезнь» (следствие гомотрансплантации клеток иммунной системы), у новорожденных — как «рант-болезнь» — болезнь малого роста (в связи с нарушением физического развития ребенка, которому имплантировали ткань, содержащую клетки иммунной системы).
АЛЛЕРГИЧЕСКИЕ РЕАКЦИИ
Аллергия — одна из форм иммунопатологических процессов, характеризующихся повышением чувствительности организма к повторным воздействиям аллергенов. Проявляется аллергия, в отличие от иммунитета, повреждением собственных тканей организма и снижением эффективности его адаптивных реакций. Это нередко приводит к тому, что носитель чужеродного антигена не разрушается до конца или не элиминируется из организма. Вместе с тем в целом аллергия, так же как и иммунитет, способствует поддержанию антигенной индивидуальности и однородности организма путем удаления из него чужеродных агентов-аллергенов.
Аллергические реакции встречаются у 10—20 % населения. Одной из причин широкой распространенности аллергии считаются «химизация» жизни современного человека, прием некоторых лекарственных препаратов, а также иногда профилактические прививки.
Аллергия формируется под воздействием аллергенов — агентов антигенной или гаптенной природы, а также некоторых физических факторов (высокой или низкой температуры, ультрафиолетового и ионизирующего излучений и др.).
Виды аллергенов
По происхождению:
Экзогенные аллергены:
- пищевые (алиментарные), к которым относятся многие продукты питания (например, шоколад, яйца, молоко, различные ягоды);
- лекарственные аллергены. Широкое применение лекарственных препаратов (особенно антибиотиков, вакцин) привело к сенсибилизации (повышенной чувствительности) миллионов людей, развитию у них аллергических осложнений и заболеваний (отеков, кожного зуда, крапивницы, анафилактического шока и др.);
- пыльцевые аллергены. Пыльца многих растений, представляющая собой комплекс белков с углеводами или пигментами пыльцы, вызывает аллергическое заболевание — поллиноз. характеризующийся преимущественным поражением дыхательных путей и слизистой оболочки глаз;
- пылевые аллергены вызывают аллергическое поражение преимущественно органов дыхания. (Бытовая пыль имеет сложный состав. В нее входят остатки органических веществ животного, растительного, микробного происхождения, синтетических тканей, пластмасс, а также неорганические соединения. Одним из наиболее активных действующих начал домашней пыли являются микроскопические клещи. Производственная пыль приобретает антигенность за счет бактериального и особенно грибкового заражения, а также примесей пестицидов, гербицидов, минеральных веществ. частиц насекомых и др.);
- эпидермальные аллергены (роговые чешуйки кожи, перьев
- птиц, частицы шерсти животных и т. п.);
- бытовые химические соединения (различные красители, стиральные порошки, кремы, косметические средства, дезодоранты и др.);
- сывороточные аллергены — препараты крови животных и человека, содержащие антитела, которые нередко используются для диагностики, лечения и профилактики различных заболеваний;
- инфекционно-паразитарные аллергены — различные микроорганизмы, вирусы, грибы, паразиты и т. д.;
- физические факторы (высокая или низкая температура, излучения с различной длиной волны и др.).
Эндогенные аллергены. К ним относятся компоненты клеток и тканей собственного организма (белки, полипептиды, крупномолекулярные полисахариды, липополисахариды), приобретающие аллергенные свойства в результате:
- действия физических, химических, инфекционных и других факторов экзогенного происхождения, приводящего к образованию в организме человека денатурированных белков или комплексов белков организма с экзогенными аллергенами (гаптенами), чаще всего с липидами, нуклеиновыми кислотами, многими лекарственными препаратами;
- повреждения клеток, становящихся мишенями для иммунной системы (например, клетки, на которых фиксируется гаптен).
По путям проникновения аллергенов в организм:
- респираторные, т. е. проникающие через дыхательные пути. Так проникают пыльца, пыль, аэрозоли, эпидермальные аллергены, некоторые лекарственные препараты и т. д.:
- алиментарные, т. е. проникающие через пищеварительный тракт. Пищевые аллергены вызывают аллергические заболевания не только органов пищеварения, но также и дыхания (аллергический ринит, бронхиальную астму), кожи и слизистых оболочек (крапивницу, аллергическую экзему и т. д.);
- «контактные» (через кожу и слизистые оболочки). Таким способом могут проникать различные низкомолекулярные вещества или местно применяемые лекарственные средства (например, мази, содержащие антибиотики), красители, древесные смолы, кремы и др.);
- парентеральные — обычно внутривенное введение препаратов крови, лекарственных препаратов, а также яды насекомых — пчел, комаров и др., попадающих в кровоток;
- трансплацентарные (некоторые лекарственные средства, например антибиотики, белковые препараты и др.).
В зависимости от вида клеток иммунной системы, принимающих участие в развитии аллергии, условно различают В-лимфоцитзависимые (гуморальные, иммуноглобулиновые) и Т-лимфоцитзависимые («клеточные») аллергические реакции.
К группе В-лимфоцитзависимых относят такие формы аллергии. в механизмах которых ведущую роль играют продуцируемые В-лимфоцитами циркулирующие в крови гуморальные антитела, принадлежащие к различным классам иммуноглобулинов — lgE, IgG, IgM. В-лимфоцитзависимые иммуноглобулиновые реакции гиперчувствительности могут быть «перенесены» от сенсибилизированного организма в другой с помощью сыворотки, содержащей эти аллергические антитела, что называется «пассивным переносом аллергии ”.
К группе Т-лимфоцитзависилых относят аллергические реакции, в патогенезе которых ведущая роль принадлежит Т-лимфоцитам и продуцируемым ими биологически активным веществам — лимфокинам. Последние выполняют роль посредников (медиаторов) в механизмах аллергии. Причинами развития таких реакций могут быть антигены чужеродных тканей и клеток, низкомолекулярные химические соединения, в том числе некоторые местно применяемые лекарственные средства (например, антибиотики), антигены микроорганизмов.
Состояние аллергии этого типа может быть «пассивно» перенесено от больного человека здоровому сенсибилизированными лимфоцитами или «экстрактом» из таких клеток, например при переливании крови или введении сывороточных препаратов.
В зависимости от скорости развития морфологических изменений и клинических проявлений после повторного действия на сенсибилизированный организма антигена (его называют «разрешающим») аллергические реакции (реакции гиперчувствительности) делят на три типа:
- реакции гиперчувствительности немедленного типа;
- реакции гиперчувствительности позднего, или отсроченного, типа;
- реакции гиперчувствительности замедленного типа.
Реакции гиперчувствительности немедленного типа проявляются сразу или через несколько минут после повторного контакта организма с аллергеном (например, аллергический ринит, конъюнктивит. анафилактический шок).
Реакции гиперчувствительности позднего типа выявляются через несколько часов (но не позднее 5—6 ч) после контакта с разрешающим антигеном (например, гемолитическая анемия аллергического генеза. некоторые разновидности сывороточной болезни).
Реакция гиперчувствительности замедленного типа регистрируются обычно через несколько часов или, чаще, суток после повторного «разрешающего» воздействия аллергена на сенсибилизированный организм (например, туберкулиновая реакция или контактный дерматит).
В зависимости от особенностей механизмов развития реакции гиперчувствительности немедленного и позднего типов развиваются в результате взаимодействия антигена с антителами сенсибилизированного организма — иммуноглобулинами. Реакция гиперчувствительности замедленного типа реализуется в основном с участием сенсибилизированных клеток — Т-лимфоцитов, их лимфокинов, а также макрофагов. Однако в патогенезе аллергических реакций участвуют механизмы, как правило, не одного, а. возможно, всех типов гиперчувствительности. И поэтому большинство болезней и реакций аллергического генеза являются комбинированными по своему механизму.
СТАДИИ И МЕХАНИЗМЫ РАЗВИТИЯ АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ
В развитии аллергии выделяют три стадии:
- I — иммуногенная (или сенсибилизации);
- II — патохимическая (образование, активация и реализация эффектов медиаторов аллергии);
- III — клинико-морфологическая (морфологические проявления аллергической реакции).
I. Иммуногенная стадия начинается с момента первого контакта аллергена с клетками иммунной системы и заключается в инициации аллергической реакции: развивается состояние сенсибилизации, т. е. повышенной чувствительности организма к данному антигену (аллергену). В этот период образуются специфические антитела или сенсибилизированные (активированные) лимфоциты к определенному антигену и накоплению их преимущественно в определенной ткани.
По механизму формирования различают активную и пассивную сенсибилизацию.
- Активная сенсибилизация развивается при попадании в организм даже минимальных количеств антигена.
- Пассивная сенсибилизация формируется после введения реципиенту сыворотки крови, содержащей специфические, сенсибилизирующие гуморальные антитела, или цельной крови, содержащей лимфоциты от активно сенсибилизированного донора.
II. Патохимическая стадия. После взаимодействия образовавшихся специфических антител или сенсибилизированных лимфоцитов с антигеном начинаются патохимические изменения в организме. В реакциях гиперчувствительности немедленного и позднего типов образование комплекса антиген—антитело в сенсибилизированном организме вызывает активацию клеточных и сывороточных протеолитических и липолитических ферментов, высвобождение клетками крови и тканей медиаторов воспаления.
При развитии аллергических реакций гиперчувствительности замедленного типа патохимическая стадия характеризуется активацией синтеза и высвобождением лимфокинов сенсибилизированными лимфоцитами.
III. Клинико-морфологическая стадия. Образующиеся при аллергизации организма гуморальные антитела и Т-лимфоциты-киллеры, взаимодействуя со свободным либо фиксированным на клетках и неклеточных структурах антигеном, вызывают прямое или опосредованное (через соответствующие медиаторы аллергии) повреждение клеток и тканей.
Для аллергии немедленного и отсроченного типов характерно быстрое развитие местных морфологических изменений вплоть до некроза тканей, а иногда и общих нарушений, включая развитие шока. К наиболее значительным изменениям такого рода относятся:
- вазомоторные реакции (местные и системные), приводящие к различным изменениям кровяного давления, регионарного кровообращения, микроциркуляции, развитию плазморрагии и фибриноидного некроза стенок сосудов;
- повышение проницаемости стенок сосудов, нередко сопровождающееся диапедезом эритроцитов и ведущее к развитию отеков, волдырей и кровоизлияний;
- спастические сокращения гладких мышечных клеток бронхиол, кишечника и других органов, что проявляется асфиксией. диспепсическими расстройствами (рвотой, диареей, болями в животе) и т. д.;
- раздражение нервных рецепторов (в основном биогенными аминами и кининами), приводящее к развитию чувства боли. зуда, жжения и т. п.
Структурно-функциональные повреждения при реакции гиперчувствительности замедленного типа связаны с развитием вначале экссудативного воспаления, которое сменяется продуктивным воспалением с выраженной мононуклеарной инфильтрацией тканей. При персистенции антигена макрофаги трансформируются в эпителиоидные клетки с образованием гранулем.
ХАРАКТЕРИСТИКА ОТДЕЛЬНЫХ ВИДОВ АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ
Анафилактический шок развивается у человека в ответ на внутривенное введение антигена, к которому организм хозяина был предварительно сенсибилизирован. Таким антигеном являются чужеродные белки, например антисыворотки, гормоны, ферменты. производные витамина В препараты из группы пенициллина, причем даже в минимальных дозах.
Развитие анафилактического шока связано с активацией IgE, который через ряд сложных реакций вызывает дегрануляцию тучных клеток и базофилов с выбросом медиаторов анафилаксии — гистамина, лейкотриенов, факторов активации тромбоцитов (ФАТ), фактора некроза опухолей (ФИО) и др. В результате развития спазма гладких мышц бронхов, желудочно-кишечного тракта нарушается дыхание, появляются боли в животе, рвота, понос. Резко повышается проницаемость сосудов с развитием отека слизистых оболочек, особенно легких, усилением секреции слизи. Появляется кожный зуд, крапивница. В финале развивается коллапс и наступает потеря сознания. Смерть может наступить в течение получаса при явлениях асфиксии, тяжелого поражения почек, печени, желудочно-кишечного тракта, сердца.
Острая крапивница и отек Квинке — проявления местной анафилаксии или атопической аллергии. Около 10% населения страдает от местной анафилаксии, возникающей в ответ на попадание в организм аллергенов — пыльцы растений, перхоти животных, домашней пыли и т. п. При этом значительно повышается проницаемость сосудистых стенок с развитием отеков, появлением мучительного кожного зуда, тошноты, болей в животе. иногда рвоты, озноба. При отеке Квинке в результате быстро нарастающего отека области шеи и лица появляются напряжение тканей, увеличение размеров губ, век, носа, ушей, языка. Наступает отек слизистой оболочки трахеи, особенно в области голосовых связок, появляется осиплость голоса и развивается асфиксия. Иногда отек распространяется на слизистые оболочки органов пищеварительного тракта с нарушением глотания и развитием острой кишечной непроходимости. Возможен отек мозга.
Острая сывороточная болезнь возникает после многократных введений чужеродной сыворотки крови при пассивной иммунизации. При этом в крови образуются иммунные комплексы антиген—антитело, которые, осаждаясь в различных тканях, вызывают воспалительные реакции. Появляются лихорадка, кожный зуд, озноб, головная боль, потливость. Иногда развиваются тошнота, рвота, боль в животе, перемежающиеся боли в суставах. Нарастающее острое воспаление сосудов, поврежденных циркулирующими иммунными комплексами (некротизирующий васкулит), проявляется появлением кожных высыпаний, поражением почечных клубочков. Продолжительность заболевания от нескольких дней до 2—3 нед.
Феномен Артюса может развиваться у больного через А—10 ч после повторного введения в то же место лекарственных препаратов («ягодичные реакции»). В области инъекций развивается экссудативно-некротическая реакция в виде некроза тканей, сопровождающегося выраженным отеком, гиперемией кожи, резкой болезненностью, кожным зудом. В основе феномена лежит экссудативно-некротическая реакция в виде фибриноидного некроза стенок сосудов, что может сопровождаться тромбозом или кровоизлиянием.
Аллергические заболевания, развивающиеся по механизму гиперчувствительности замедленного типа (клеточно-опосредованного). Эти заболевания вызывают специфически сенсибилизированные Т-лимфоциты, прежде всего СД4 и СД8 (т. е. Т-лимфоциты-супрессоры и Т-лимфоциты-киллеры). Это основной тип иммунного ответа на внутриклеточные микробные агенты, особенно микобактерии туберкулеза, а также на многие вирусы, грибы, простейшие, паразиты. Примером такой реакции служит реакция на внутрикожно введенный туберкулин — компонент стенки микобактерии туберкулеза. У пациента, уже сенсибилизированного микобактерией туберкулеза, через 8—12 ч возникает покраснение и уплотнение в месте введения туберкулина, а пик реакции наступает через 24—72 ч, когда в дерме и подкожной клетчатке накапливаются мононуклеарные клетки, преимущественно вокруг венул, образуя периваскулярные манжетки. При этом преобладают Т-лимфоциты (СД4). В зоне инъекции может развиваться некроз.
Болезни иммунной аутоагрессии (БИА), или аутоиммунные болезни. К ним относят нарушения жизнедеятельности организма, вызванные развитием иммунопатологических реакций, направленных против собственных клеток и неклеточных структур. Сущность этих заболеваний заключается в потере клетками и тканями организма аутотолерантности.
Конкретные причины и механизмы отдельных аутоиммунных заболеваний сложны и еще недостаточно изучены. К числу наиболее исследованных механизмов происхождения БИА относят:
- БИА обусловленные патологическими изменениями в системе иммунобиологического надзора (мутацией пролиферирующих иммуноцитов, расстройством оптимального соотношения количества или активности Т-, В-лимфоцитов-сугрессоров и Т-лимфоцитов-хелперов, отменой невосприимчивости Т-лимфоцитов к аутоантигенам, антигеннеспецифической поликлональной активацией лимфоцитов);
- БИА вызванные патологическими изменениями вне системы иммунобиологического надзора [отсутствием естественной толерантности к собственным антигенным структурам, изменением антигенов организма, мутацией (изменением) генома отдельных клеток организма, внедрением экзогенных антигенов, сходных с собственными антигенами].
БОЛЕЗНИ ИММУННОЙ АУТОАГРЕССИИ
В зависимости от доминирующего механизма развития выделяют:
- болезни иммунной аутоагрессии, развивающиеся в основном с участием иммуноглобулинов, например тиреоидит Хашимото, гемолитическая анемия, тромбоцитопения, лейкопения, системная красная волчанка;
- аутоиммунные болезни, развивающиеся в основном с участием Т-киллеров, например отдельные разновидности полимиозита и синдрома Шегрена;
- аутоиммунные болезни, развивающиеся с участием обоих звеньев иммунного ответа, например синдром Шегрена, при котором происходит поражение слезных, слюнных, слизистых и др. желез, проявляющийся поражением глаз (сухой кератоконъюнктивит), слизистой оболочки рта (ксеростомия);
- склеродермия;
- дермато- и полимиозит.
В зависимости от числа пораженных органов различают моноорганные (или органоспецифические аутоиммунные болезни) и полиорганные БИА (син.: системные, генерализованные).
При люноорганных БИА аутоагрессивные Т-киллеры или специфические антитела взаимодействуют с антигенными структурами только одного органа.
Примерами являются тиреоидит Хашимото и анемия Аддисона—Бирмера (пернициозная). При тиреоидите Хашимото иммуноглобулины (антитела) строго специфичны по отношению к антигену — белку щитовидной железы тиреоглобулину. В результате этого взаимодействия гибнет функциональная ткань щитовидной железы.
В случае анемии Аддисона—Бирмера в крови выявляются аутоагрессивные иммуноглобулины к измененному внутреннему фактору Касла — гастромукопротеину, образующемуся в слизистой оболочке желудка и являющемуся важнейшем звеном регуляции гемопоэза.
При полиорганных БИА действие аутоиммунных Т-киллеров и антител направлено против антигенных структур многих органов и тканей организма.
Причины: наличие у них сходного антигена, низкая специфичность аутоагрессивных Т-лимфоцитов и антител. Примером может служить системная красная волчанка, при которой аутоиммуноглобулины (аутоантитела) взаимодействуют с определенными антигенами ядер и цитоплазмы клеток многих тканей и органов, в том числе полиморфно-ядерных лейкоцитов.