В статье в соответствии с методами доказательной медицины приводится обзор современных данных по терапии расстройств тревожного спектра. Кратко излагаются эпидемиология и различные варианты медикаментозной терапии тревожных расстройств, включая антидепрессанты, транквилизаторы, атипичные антипсихотики, антиконвульсанты и бета-блокаторы. Дается анализ сравнительных рандомизированных контролированных исследований по эффективности этих групп препаратов при паническом расстройстве, генерализованном тревожном расстройстве, социальном тревожном расстройстве и посттравматическом стрессовом расстройстве. На основе анализа данных литературы предложены клинические рекомендации терапии всех тревожных расстройств. Тревожные расстройства (ТР) наиболее распространены среди психических расстройств. Так, 30-40% населения перенесли в жизни хотя бы один тревожный эпизод. Распространенность панического расстройства (ПР) колеблется от 1,5% до 3,5%, социального тревожного расстройства (СТР) — от 2,4% до 13,3% и генерализованного тревожного расстройства (ГТР) — от 4,1 % до 6,6% (Kessler R. et al., 1994; Wittchen H. et al., 2001; Lepine J., 2002). Однако, проблема TP не только в их высокой распространенности, но и в частой, до 75 %, коморбидности с другими психическими расстройствами. Причем коморбидность в случае с ТР не ограничивается одним заболеванием. Так, коморбидность с тремя другими психическими расстройствами в случае ПР составляет — 23,5 %, обсессивно-компульсивного расстройства (ОКР) — 23 %, а посттравматического стрессового расстройства (ПТСР) — 27 % (Nutt D., Ballenger J., 2003). Несмотря на высокую распространенность ТР, только около 30 % больных активно ищет помощи. Кроме того, ТР в значительной степени окрашены этническими и культуральными особенностями, в связи с чем в значительной степени затруднена стандартизация их диагностики и лечения. Поэтому пациенты, страдающие ТР, редко получают своевременную и адекватную медицинскую помощь. Важной проблемой является также тот факт, что пациенты часто обращаются не к психиатрам, а к врачам общей практики, которые нередко не обладают достаточной квалификацией для диагностики и терапии ТР и не воспринимают их как серьезное медицинское заболевание (Краснов В.Н., 2001). В таблице 1 приведены дифференциальные критерии ТР как медицинского заболевания от тревоги как психо-социального феномена (Swinson R. et al., 2006)
Когда тревога становится заболеванием?
- Тревога имеет большую интенсивность и (или) продолжительность, чем обычно ожидается, учитывая обстоятельства её развития (в контексте семейного, общественного и культурного поведения)
- приводит к потере трудоспособности или инвалидности, снижению профессиональной, социальной активности или межличностного функционирования
- затрудняет ежедневную деятельность из-за невозможности определенных ситуаций или неэффективных действий в попытках уменьшить проявления тревоги (поведение избегания, ритуалы)
- включает клинически значимые, необъяснимые физические симптомы и (или) навязчивости, побуждения и воспоминания или воспоминания травмы
Ситуация с людьми, страдающими тревожными расстройствами, в нашей стране драматически осложнена тем фактом, что пациентам с тяжелым и длительным течением ПР или ОКР ставится диагноз вялотекущей шизофрении и назначается нейролептическая терапия. Серьезной проблемой отечественной психиатрии является недостаточное развитие психотерапии как эффективного и равноправного метода лечения расстройств тревожного спектра, так же как недостаточное понимание специалистами в области душевных расстройств, не имеющих медицинского образования, важности фармакотерапии тревожных расстройств (Холмогорова А. Б., 2010). Изучение психотерапии ТР было начато еще в конце XIX века 3. Фрейдом, однако, долгое время серьезные различия в подходах к терапии и недостаточность доказательной базы мешали её признанию как высокоэффективного метода терапии ТР в медицинском мире. Эффективность когнитивно-бихевиоральной психотерапии была показана в многих рандомизированных контролированных исследованиях (РКИ) и мета-анализе 108 исследований (Norton Р. et al., 2007, Барлоу Д., 2010).
За полвека существования психофармакотерапии несколько классов психотропных препаратов хорошо зарекомендовали себя при лечении ТР. Терапия расстройств тревожного спектра имеет общие принципы, так как ТР имеют родственный патогенез (чем, по-видимому, и обусловлена высокая коморбидность этих состояний), связанный с поражением серотониновой и ГАМК-ергической систем головного мозга. Селективные ингибиторы обратного захвата серотонина (СИОЗС) СИОЗС являются препаратами первого выбора для лечения всех ТР, включая ОКР, ПТСР и изолированные фобии, а также при коморбидности ТР с депрессией. Возможность патогенетического воздействия СИОЗС на тревожную симптоматику и депрессию, а также благоприятный профиль переносимости сделали эту группу препаратов наиболее назначаемой при ТР. Анксиолитический эффект СИОЗС развивается, как правило, на 2-4-й неделе терапии. Лечение СИОЗС хорошо переносится, однако в первые дни или недели лечения могут возникать такие симптомы, как беспокойство, усиление тревоги, бессонница, головная боль, что может повлиять на желание пациентов принимать назначенный препарат. Понижение стартовой дозы СИОЗС (особенно в случае терапии ПР) может значительно уменьшить эти симптомы, являющиеся следствием избыточной стимуляции серотониновых рецепторов. Другие возможные побочные эффекты включают, прежде всего, головокружение, тошноту, анорексию или увеличение веса. При долгосрочном лечении могут стать проблемой сексуальная дисфункция (снижение либидо, импотенция или нарушения эякуляции); также наблюдался синдром отмены, особенно при использовании пароксетина (Bandelow В. et al., 2002). Селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) Эффективность СИОЗСН, венлафаксина и дулоксетина при ТР была продемонстрирована в нескольких РКИ (см. ссылки по отдельным расстройствам). Противотревожный эффект, также как и в случае с СИОЗС, развивается через 2-4 недели терапии. В начале лечения побочные эффекты, такие как тошнота, беспокойство, бессонница или головная боль, могут привести к отказу от терапии. Трициклические антидепрессанты (ТЦА) Эффективность ТЦА в лечении большинства тревожных расстройств хорошо доказана, главным образом, для имипрамина и кломипрамина (см. ссылки по отдельным расстройствам). В сравнении с антидепрессантами нового поколения эффективность лечения, может быть снижена неблагоприятными эффектами, такими как первоначальное усиление тревоги, сухость во рту, постуральная гипотензия, тахикардия, седация, сексуальные дисфункции, повышение веса. Длительному приему ТЦА могут мешать ограничения на вождение автомобиля, что является достаточно серьезной проблемой в связи с длительным назначением противотревожной терапии. Резкое прекращение терапии ТЦА может также вызывать синдром отмены, а фармакокинетические взаимодействия могут ограничить их использование у пациентов, принимающих сопутствующее лечение. У пожилых пациентов следует мониторировать появление сердечно-сосудистых побочных эффектов. Применения ТЦА следует избегать у пациентов с риском самоубийства из-за их потенциальной кардио- и ЦНС-токсичности при передозировке (Nutt D., 2005).
Транквилизаторы Эффективность бензодиазепинов (БД) при ТР показана в нескольких рандомизированных клинических исследованиях. Анксиолитический эффект наступает быстро, у некоторых препаратов уже через 30-60 минут после перорального или парентерального применения. В отличие от антидепрессантов их назначение не приводит к первоначальному усилению тревоги или панических переживаний. БД хорошо переносятся, однако могут приводить к формированию зависимости, вызывать седацию и когнитивные нарушения (Livingston М., 1994). Лечение БД при краткосрочном использовании является эффективным, достаточно безопасным и находится вне конкуренции на начальном этапе терапии ТР, когда скорость и глубина редукции тревожной симптоматики являются приоритетной задачей. Однако поддерживающая терапия ТР не рекомендуется из-за возможности формирования зависимости с необходимостью постоянного увеличения эффективной дозы. Поэтому длительная терапия транквилизаторами показана только пациентам, для которых другие методы терапии оказались неэффективны или приводили к серьезным побочным эффектам. Назначение БД пациентам с алкоголизмом или наркоманией в анамнезе не рекомендуется в связи с высоким риском возникновения зависимости (Spiegel D., 1999). В настоящее время для лечения ТР БД обычно применяются в комбинации с антидепрессантами в течение первых недель с целью быстрого купирования тревоги (Goddard A. et al., 2001). Буспирон (азапирон), являющийся 5-НТ1А-агонистом, может быть эффективным при лечении ГТР, как показано в нескольких РКИ (см. ссылки по отдельным расстройствам). При других ТР результаты РКИ были преимущественно отрицательными. Антигистаминный препарат гидроксизин (атаракс) был эффективен при ГТР (см. ссылки ниже). Из-за седативных эффектов антигистаминные препараты следует использовать только когда лечение другими лекарственными средствами не было успешным или плохо переносилось. Опыт долгосрочного лечения недостаточен. Эффективность гидроксизина при других ТР не доказана. Одним из последних анксиолитиков, появившихся на рынке, стал отечественный препарат афобазол. Препарат был разработан в НИИ фармакологии РАМН и явился результатом поиска селективных анксиолитиков, лишенных побочных эффектов, характерных для БД. По химической структуре афобазол относят к производным меркаптобензимидазола. Его действие препятствует развитию мембранозависимых изменений в ГАМК-рецепторах, что снижает доступность соответствующего лиганда. Афобазол имеет короткий период полувыведения, который составляет 0,82±0,54 часа. К настоящему времени в открытых исследованиях получены данные о его эффективности при ГТР на этапе активной купирующей терапии (Аведисова А. С. с соавт., 2006; Незнанов Г. Г. с соавт., 2006) и при длительном применении (Аведисова А. С. с соавт., 2008). В этих исследованиях афобазол показал эффективность, сопоставимую с диазепамом, при лучшей переносимости. Однако отсутствие РКИ по оценке эффективности препарата при ТР существенно ограничивает доказательную базу и не позволяет рекомендовать афобазол среди препаратов первого выбора при лечении ТР.
Атипичные антипсихотики (АА) Начиная с 70-х годов, ТР часто лечили типичными нейролептиками, такими как галоперидол, флуспирилен, флупентиксол, сульпирид, хлорпротиксен, тиоридазин и др. в более низких дозах, чем они используются при лечении шизофрении. Однако, наличие серьезных экстрапирамидных и нейроэндокринных побочных эффектов, возможность отдаленных нежелательных явлений привели в настоящее время к практически полному отказу от использования традиционных нейролептиков при терапии ТР. Появление группы АА в последние годы изменило это тенденцию. Во многих исследованиях АА использовались для усиления (аугментации) лечения антидепрессантами резистентных случаев ТР (LaLonde С., Van Lieshout R., 2011). Антиконвульсанты Антиконвульсанты, включая карбамазепин, вальпроат, ламотриджин, топирамат, прегабалин и габапентин, показали неплохую эффективность в отдельных РКИ (см. отдельные ТР) и заслуживают дальнейшего изучения. Однако, широкий опыт их использования в клинической практике отсутствует. Исключением является прегабалин, открытие противотревожного действия которого является значительным достижением последних лет в области терапии ТР. Механизм действия прегабалина отличается от эффектов как бензодиазепинов (они повышают активность ГАМК-содержащих промежуточных нейронов, обеспечивающих ингибирующую модуляцию всей ЦНС), так и различных тимоаналептиков (ТЦА, СИОЗС, СИОЗСН), блокирующих механизм обратного захвата моноаминов (серотонина, норадреналина и дофамина). Анксиолитическое действие прегабалина обусловлено его связыванием с субъединицей а2-d-протеин класса кальциевых каналов, расположенных в пресинаптической области, отвечающих за высвобождение нейротрансмиттеров. Прегабалин действует за счет механизма, сходного с механизмом габапентина, пресинаптического ингибитора высвобождения глутамата, аспартата и субстанции Р. Потенциалзависимые кальциевые каналы в ЦНС обеспечивают быстрое блокирование высвобождения нейротрансмиттера, контролируя присоединение синаптических пузырьков к пресинаптическим мембранам.
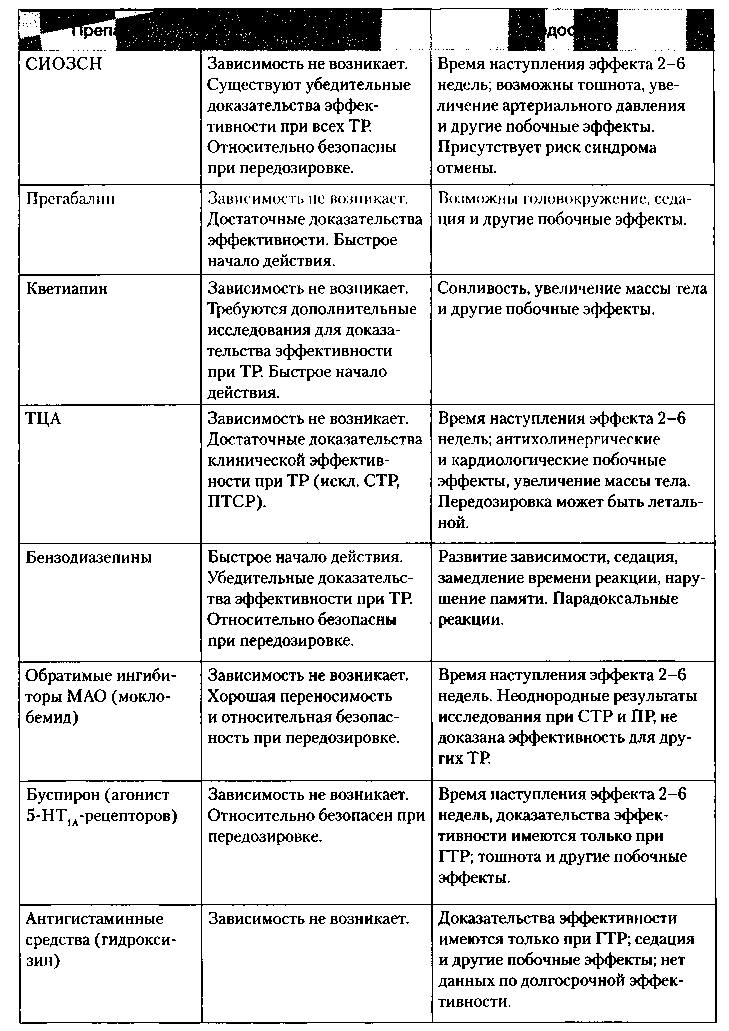
Прегабалин продемонстрировал эффективность при лечении нейропатических болей, различных форм эпилепсии и ряда ТР. Наиболее изучено его действие при терапии ГТР. Однако ведутся исследования по изучению эффективности прегабалина при терапии других расстройств тревожного спектра. Так, уже есть отдельные данные о целесообразности его применении при СТР и ПР. Основные побочные эффекты прегабалина включают головокружение, седацию, сухость во рту, амблиопию, ослабление координации и снижение психомоторной и когнитивной функций. В доклинических и клинических исследованиях не наблюдалось случаев формирования зависимости. Адренергические бета-блокаторы Способность бета-блокаторов влиять на вегетативные проявления тревоги используется в лечении тревожных расстройств довольно давно. Однако доступные двойные слепые контролируемые исследования не подтвердили эффективность бета-блокаторов при различных ТР. Кроме того, пациенты с тревожными расстройствами нередко страдают от колебаний сосудистого тонуса, и эти состояния могут усугубляться бета-блокаторами. В настоящее время этой группе препаратов отводится вспомогательное значение при терапии ТР. Ни один из доступных медикаментозных видов лечения не является идеальным для индивидуального пациента. В таблице 2 перечислены достоинства и недостатки наиболее распространенных групп препаратов, применяющихся для терапии расстройств тревожного спектра.
| Препарат | Преимущества | Недостатки |
| СИОЗС | Зависимость не возникает.
Существуют убедительные доказательства эффективности при всех ТР Относительно безопасны при передозировке. |
Время наступления эффекта 2-6 недель, возможны начальная тревога, тошнота, психомоторное возбуждение, сексуальные дисфункции и другие побочные эффекты. У ряда препаратов существует опасность синдрома отмены. |
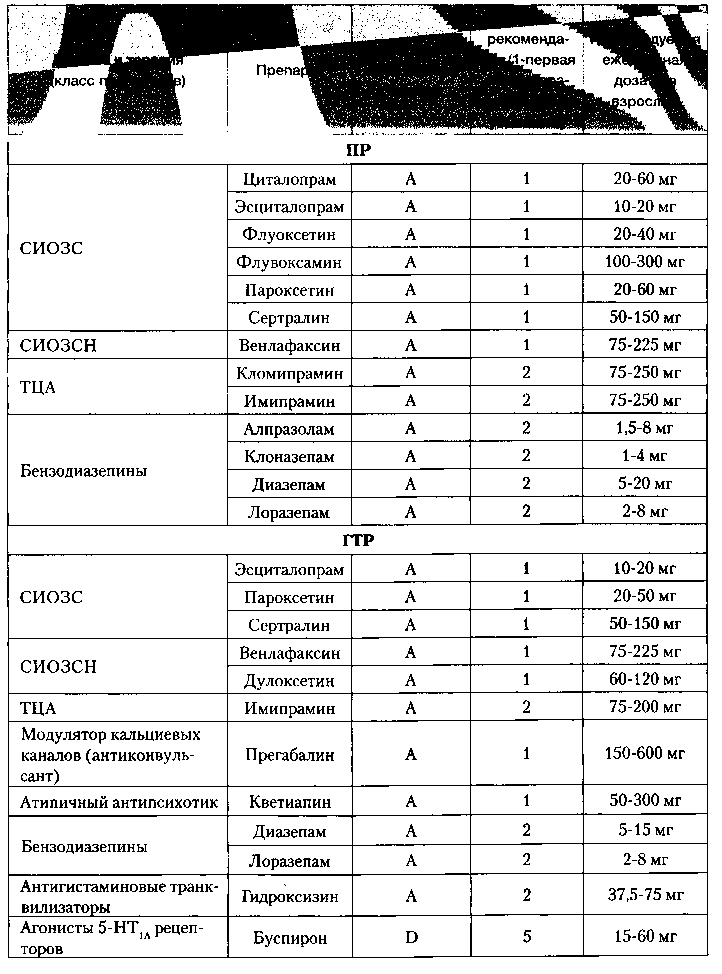
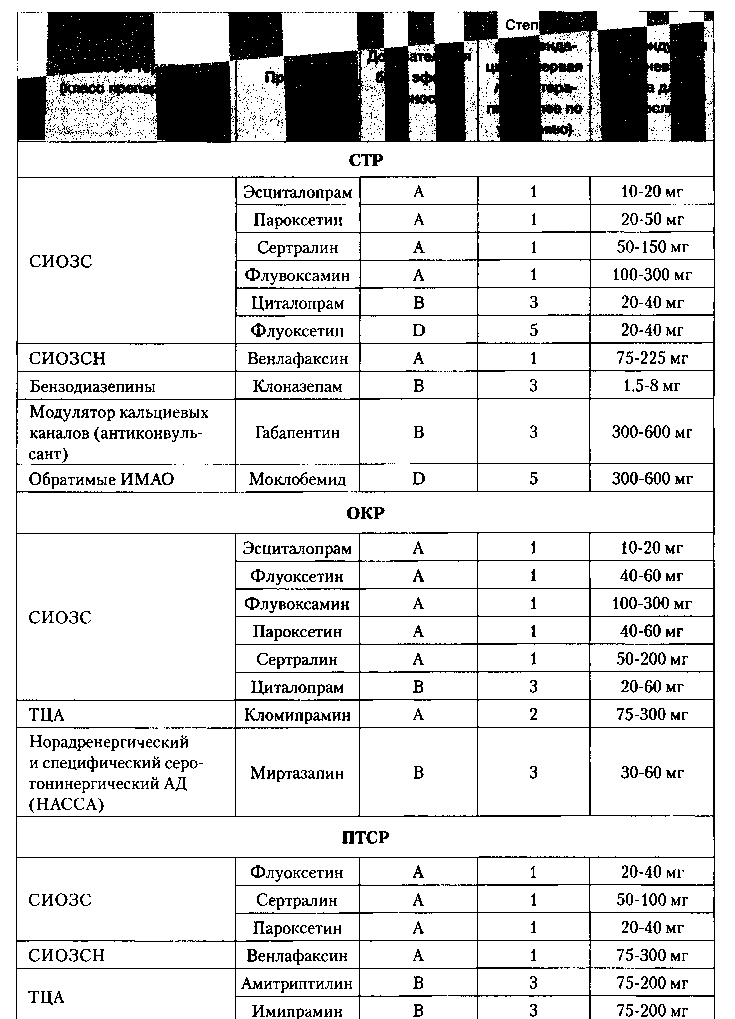
Таблица 3. Рекомендации для медикаментозного лечения тревожных расстройств (апаптировано по Bandelow В. et al., 2008)
- А — наиболее достоверные данные, доказательства получены на основании нескольких рандомизированных двойных слепых плацебо контролируемых исследованиях и/или в мета-анализе нескольких РКИ;
- В — ограниченные положительные доказательства, полученные хотя бы в одном РКИ;
- С — доказательства из неконтролируемых исследований или исследований с описанием серии случаев/мнения экспертов;
- D — неоднородные результаты, положительные РКИ сопровождаются приблизительно равным количеством отрицательных исследований.