В статье в соответствии с методами доказательной медицины приводится обзор современных данных по терапии обсессивно-компульсивного расстройства (ОКР). Кратко излагаются эпидемиология, патогенез, основные клинические проявления, течение, прогноз и дифференциальная диагностика ОКР. Подробно рассматривается ведущая серотонинергическая гипотеза развития заболевания. Главное внимание уделяется обзору доказательных исследований по различным аспектам лекарственной терапии ОКР, прежде всего применению ингибиторов обратного захвата серотонина. Приводятся психометрические методы диагностики и отслеживания динамики и симптоматики ОКР в процессе терапии. На основе анализа данных литературы и собственного опыта предложен оригинальный алгоритм лечения ОКР.
Распространенность обсессивно-компульсивного расстройства (ОКР) в общей популяции составляет 2-3% (Rasmussen S.A., Tsuang М.Т., 1984; Wiseman М.М. с соавт., 1994; Тиганов А. С., 1999). Заболевание встречается примерно в равной мере у мужчин и женщин и обычно начинается в подростковом возрасте (одна треть случаев в возрасте до 15 лет). Более чем у половины больных ОКР впервые появляется в возрасте до 21 года (в среднем — 19,8±1,9 лет). Общие затраты общества (прямые и непрямые расходы) по лечению больных ОКР в США в 1993 году составили 8,4 миллиардов долларов (Dupont R. с соавт., 1995).
В целом вопрос об этиологии и патогенезе ОКР остается недостаточно ясным. Нейробиологическая теория ОКР поддерживается многочисленными фактами выявления у больных различных неврологических расстройств, включая травмы головного мозга, в том числе родовые, эпилепсию, хорею Сиденхэма и хорею Гентингтона. При обследовании нередко обнаруживаются патология на ЭЭГ и отклонения при нейропсихологическом тестировании. У детей был также описан особый вариант ОКР после ^-стрептококковой инфекции группы А. В настоящее время накопилось большое количество данных, указывающих на нарушения в структурах, контролируемых серотонинергической системой. Недавние исследования с помощью техники позитронно-эмиссионной томографии (ПЭТ) обнаружили заинтересованность у этих больных орбитальной извилины лобных долей и лимбических структур мозга, т. е. областей, богатых серотонинергическими нейронами, а также хвостатого ядра. Усиленный метаболизм глюкозы в этих структурах исчезал после курса лечения селективными ингибиторами обратного захвата серотонина (СИОЗС) (Baxter L. R. с соавт., 1992; Gross R. с соавт., 1998 и др.)
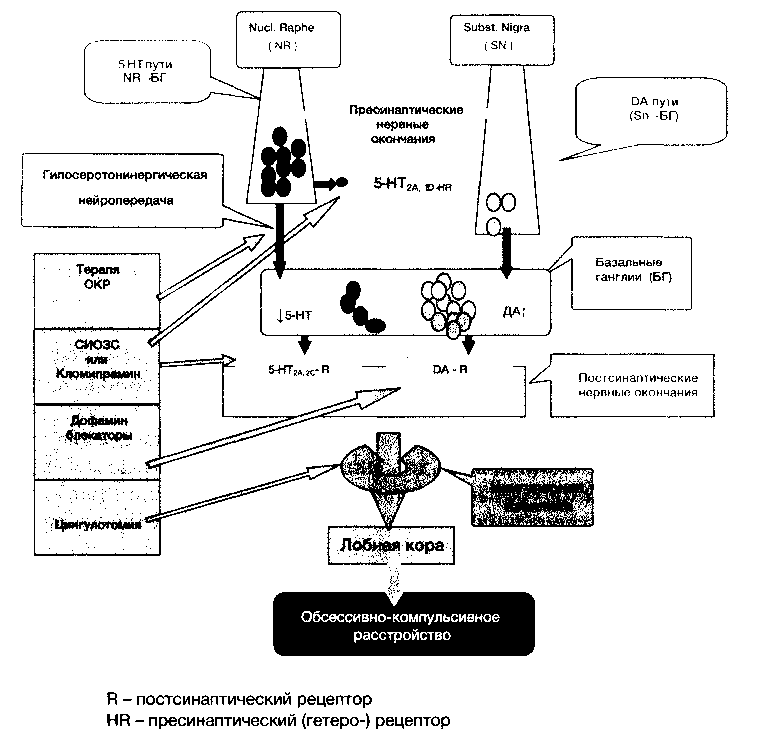
В последние годы появляется все больше данных о том, что в патогенез ОКР вовлечена также дофаминовая система. Клиническими фактами, подтверждающими это, являются высокая коморбидность ОКР с синдромом Туретта (40-60 %), а также тесная связь стереотипного поведения с непроизвольными движениями. При этом взаимодействие двух систем происходит, по-видимому, на уровне базальных ганглиев, в которых пересекаются как серотониновые пути из ядра шва среднего мозга, так и дофаминовые пути из substantia nigra. На этом уровне серотониновые нейроны оказывают модулирующее (угнетающее) действие на дофаминергическую нейропередачу путем воздействия на находящиеся на дофаминовых нейронах серотониновые ауторецепторы. При нормальной функции серотонинергической системы происходит ограничение активности дофаминергической нейропередачи. При уменьшении выброса серотонина способность к угнетению дофаминергической нейропередачи снижается, вследствие чего между системами развивается дисбаланс и дофаминовая активность в базальных ганглиях становится доминирующей. Этим можно объяснить развитие некоторых симптомов ОКР, в частности, стереотипное поведение и моторные нарушения. Из базальных ганглиев эфферентные серотонинергические пути через цингулярную извилину идут в корковые структуры, в том числе лобную кору, с поражением которой связывают развитие идеаторных навязчивостей (Shiloh R. с соавт., 1999).
Несомненное значение имеют и наследственно-генетические факторы. Конкордантность расстройства выше у монозиготных близнецов, чем у дизиготных пар. Частота встречаемости навязчивостей у ближайших родственников больных в 2 раза выше, чем в популяции (DSM-IV, 1994). Примерно у 20-30% родственников I линии обнаруживаются симптомы обсессивно-компульсивного спектра. Кроме того, у них нередко встречаются другие тревожные и аффективные расстройства, а также синдром Туретта (Stein D.J., Hollander Е„ 2002).
Психодинамически ориентированные специалисты традиционно объясняют ОКР фиксацией на генитальной стадии развития и регрессом к ранней анальной стадии, которая связана с представлениями о грязи, магическим мышлением, амбивалентностью и др. Это приводит к гипертрофии суперэго и включает различные защитные механизмы для преодоления тревоги. Хотя навязчивости и ритуалы часто бывают наполнены символическим содержанием, психодинамический подход не является эффективным методом лечения этого заболевания и в настоящее время имеет преимущественно исторический интерес.
Специалисты поведенческой психотерапии объясняют развитие ОКР в терминах теории обучения. Они считают, что первичной причиной является возникновение тревоги в период с какими-то конкретными событиями (например, загрязнение или заражение), которая закрепляется по типу простого условного рефлекса. Для облегчения тревоги больной совершает ритуальные действия, которые в случае успеха также закрепляются по условнорефлекторному типу. Хотя экспериментальными исследованиями эта теория не подтверждается, поведенческая психотерапия в настоящее время является одним из ведущих психотерапевтических методов коррекции ОКР.
Обсессии (навязчивости) представляют собой вызванные длительным тревожным аффектом и стереотипно повторяющиеся идеи, образы или влечения, которые воспринимаются больным как собственные, часто бессмысленные или даже абсурдные мысли и которым он стремится сопротивляться различными способами, в том числе с помощью защитных действий (ритуалов или компульсий). Последние также воспринимаются как бессмысленные и чрезмерные, но повторяются больным для уменьшения выраженности нарастающей тревоги вследствие навязчивых представлений. В целом, идеаторный, аффективный и поведенческий компоненты ОКР неразрывно связаны друг с другом и развиваются по типу порочного круга (см. рис. 1). Тем не менее у некоторых больных компульсии не всегда сопровождают навязчивости и не всегда представляют собой защитное поведение (двигательные акты). Например, компульсии могут обнаруживаться в виде мысленного счета. Обсессии и компульсии, как правило, тягостно переживаются больным, т. е. имеют эгодистонический характер, и приводят к снижению уровня социального функционирования.
Обсессивно-компульсивное расстройство в определении современных диагностических критериев характеризуется навязчивыми мыслями (обсессии) или навязчивыми действиями ритуалами (компульсии), а чаще всего их сочетанием (80%). Эпидемиологические исследования показывают, что в отличие от прежних представлений только у 10% больных эти нарушения вытекают из особого невротического (ананкастного) склада личности (склонности к сомнениям, стремлению к порядку, перфекционизма, педантичности, ригидности, излишнем внимании к деталям и т. д.) (Rasmussen S. A., Tsuang М. Т., 1984; Montgomery S. А., 1993). Более часто (около 40%) ОКР встречается у зависимых, истерических и уклоняющихся личностей. Эта диагностическая категория в целом соответствует понятию невроза навязчивых состояний в отечественной психиатрии, хотя часть случаев упорных навязчивостей крайне вычурного и абстрактного характера, так называемый шизообсессивный вариант (Zohar J. et al., 2000), по-видимому, более обоснованно рассматривать в рамках вялотекущей неврозоподобной шизофрении (шизотипического расстройства личности).
S. A. Rasmussen и M.T. Tsuang (1984) произвели оценку частоты встречаемости различных видов навязчивостей среди больных, удовлетворяющих современным диагностическим критериям. При этом оказалось, что наиболее часто встречались навязчивости загрязнения (мизофобия) (55%), агрессивные навязчивые импульсы (50%), навязчивые желания в отношении симметричности и точности расположения предметов (37 %), соматические навязчивости (35 %). Среди компульсий наиболее часто встречались действия по проверке сделанного (79%), мытья и чистки (58%) и счета (21 %). Авторы обнаружили преобладание компульсий мытья и чистки среди женщин. У многих больных развивается поведение избегания ситуаций, соответствующих их навязчивостям. Так, больные со страхом загрязнения избегают пользоваться публичными туалетами или рукопожатий с незнакомыми людьми. Нередко встречаются ипохондрические жалобы на свое здоровье с частым посещением врачей. У некоторых больных вследствие личностных черт повышенной ответственности присутствует чувство вины.
Все эти признаки сближают навязчивости с другими диагностическими категориями (например, социальной фобией, соматоформными расстройствами или депрессией), что требует внимательной оценки состояния больного при постановке диагноза. Диагностика также затрудняется тем, что больные неохотно делятся с врачом своими переживаниями. Поэтому нередко требуется проведение прицельного расспроса. Разрыв между первыми симптомами заболевания и правильным установлением диагноза с началом адекватной терапии достаточно велик и, например, в американской популяции в среднем составляет 17 лет (см. рис. 2). Заболевание развивается постепенно и, как правило, приобретает хронический волнообразный характер с периодическим усилением или ослаблением симптоматики, что часто бывает связано со стрессовой провокацией. У 65% больных течение имеет неблагоприятный, прогрессирующий характер и приводит к значительному нарушению социально-трудовой адаптации, у 5 % больных, напротив, наблюдается эпизодическое течение с полным отсутствием симптоматики в ремиссиях (DSM-IV, 1994). Только у 10% больных отмечаются спонтанные ремиссии длительностью более года.
Хотя при проведении адекватной терапии выраженность навязчивостей может существенно редуцироваться, прогноз у большинства больных в целом не очень благоприятный. Заболевание, как правило, имеет хронический рецидивирующий характер. Прогноз может быть лучше, если заболевание началось в более позднем возрасте, уровень преморбидной адаптации был достаточно высокий, а симптомы заболевания выражены умеренно или легко. При раннем начале и наличии личностных нарушений прогноз значительно ухудшается. Вычурные навязчивости или ритуальные действия, а также присоединение выраженных компульсий и отсутствие сопротивления им также ухудшают прогноз течения. Существенно осложняет течение ОКР присоединение депрессии, которая, по некоторым данным, наблюдается почти у 80 % больных. Суицидальные идеи достаточно часты при идеаторных навязчивостях, однако редко приводят к суициду.
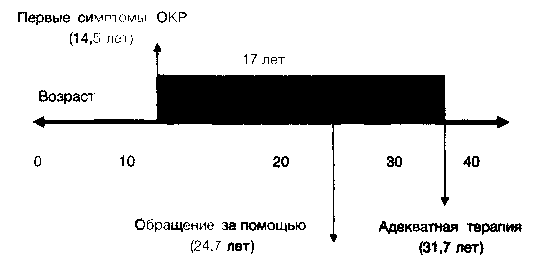
Рис. 2. Разница между развитием начальной симптоматики и назначением адекватной терапии (по Hollander Е., 1993)
В последнее время в связи с успехами применения антидепрессантов — ингибиторов обратного захвата серотонина активно разрабатывается концепция расстройств обсессивно-компульсивного спектра, при которых также постулируется серотонинергический дефицит (Hollander Е., 1993; Me Elroy S., 1994; Koran L. М., 1999; Hollander Е., Simeon D., 2003). По некоторым данным, расстройствами обсессивно-компульсивного спектра страдает до 10% населения (Koran L. М., 1999; Hollander Е., Simeon D., 2003).
К этим расстройствам относятся дисморфофобия, расстройства пищевого поведения (нервная анорексия и булимия), ипохондрический синдром, тики (синдром Туретта, хорея Сиденхэма), импульсивные действия — трихотилломания, перемежающееся эксплозивное расстройство (вспышки агрессивности), клептомания, кусание ногтей (онихофагия), пощипывание кожи, влечение к покупкам (ониомания), к азартным играм (патологические игроки), пиромания, самоповреждающие действия, сексуальное агрессивное поведение, включая сексуальные извращения и т. д.), а также ряд феноменологически сходных, пограничных с обсессивно-компульсивными нарушениями состояний (детский аутизм, стереотипии, ритуальное поведение, сенестопатии, деперсонализационный синдром, катаплексия, ананкастные личностные черты, малые психические автоматизмы Клерамбо и др.). При всех этих разнообразных и нозологически неоднородных, с точки зрения отечественной психиатрии, состояниях помогают СИОЗС (Kafka М. Р., 1991; Emmanuel N. Р. с соавт., 1991; Barsky A.J., 1992; Swedo S. Е., Leonard Н. L., 1992; Hollander E. с соавт., 1993; Swedo S. E., 1994 и др.).
В соответствии с современной классификационной концепцией нередко состояние одновременно отвечает диагностическим критериям нескольких категорий (коморбидность) — наиболее часто это рекуррентная депрессия (50-70%), соматоформное расстройство (30-40%), специфические или простые фобии (20-30%), паническое расстройство (20-30%), социальная фобия (20-25%), шизофрения (10-15%), а также синдром Туретта, хорея Сиденхэма и постэнцефалический паркинсонизм, при которых навязчивости встречаются у 35-50% больных (DSM-IV, 1994). Примерно у 20-30% больных ОКР отмечаются тики. У 10-15% больных ОКР сопровождается алкоголизмом и другими токсикоманиями, у 5 % наблюдается биполярное расстройство.
Специальное исследование, посвященное коморбидности ОКР и депрессии, показало, что у 80 % больных наблюдалась депрессивная симптоматика, однако в большинстве случаев она развивалась после начала навязчивостей, т. е. носила вторичный характер (Rasmussen S. A., Tsuang М.Т., 1984). При первичной депрессии с навязчивым мышлением („умственной жвачкой») имеется отчетливая связь с депрессивными переживаниями, неотступные идеи вины, греховности. Эти мысли воспринимаются больным как естественные, хотя может быть преувеличенные, и без сопротивления. В отличие от обсессий при депрессии навязчивые мысли, как правило, направлены в прошлое. Навязчивости при депрессии носят транзиторный характер и полностью исчезают вместе с депрессией. При дифференциальной диагностике, помимо последовательности развития ведущей симптоматики, нужно также обращать внимание на дисфорический оттенок тревоги и эгодистонический характер навязчивостей при ОКР.
Современная терапия навязчивых состояний должна обязательно предусматривать комплексное (психотерапевтическое и фармакотерапевтическое) воздействие. При этом основными задачами лечения являются редукция тревоги, разрешение внутреннего конфликта и достижение эффективных путей выхода из стресса. Среди всех классов психотропных средств наибольшую эффективность обнаружили антидепрессанты. Многочисленные исследования показали, что применение бензодиазепинов и нейролептиков оказывает в основном симптоматический (анксиолитический) эффект, но не влияет на ядерную обсессивную симптоматику. Более того, экстрапирамидные побочные эффекты классических нейролептиков могут привести к усилению навязчивостей.
Среди антидепрессантов при обсессивно-компульсивном расстройстве используются три группы препаратов: ингибиторы МАО (ИМАО); трициклические антидепрессанты (ТЦА); селективные ингибиторы обратного захвата серотонина (СИОЗС) и норадреналина (СИОЗСН). Ингибиторы МАО применялись с определенным результатом для лечения навязчивостей, начиная с 60-х годов, и в настоящее время больше имеют исторический интерес. Наиболее часто из них использовались фенелзин (нардил), транилципромин (трансамин, парнат) и ниаламид (нуредал) (Rihmer Z. с соавт., 1982; Jenike М. А. с соавт., 1989; 1997; Valejo J. с соавт., 1992 и др.).
Среди положительных предикторов эффективности ингибиторов МАО при ОКР были обнаружены панические атаки и выраженная тревога. Напротив, так называемое „шизотипическое расстройство личности» имело отрицательное прогностическое значение (Jenike М. А., 1989). Эти исследования были выполнены по открытому принципу, без надлежащего плацебо-контроля, на небольшом количестве больных, поэтому глобальная эффективность ИМАО при ОКР остается неясной. Кроме того, применение необратимых ингибиторов МАО всегда связано с высоким риском тяжелых побочных явлений и лекарственных взаимодействий. Возможности селективных обратимых ингибиторов МАО при этих состояниях не определены.
В настоящее время большинство исследователей полагает, что наилучшего эффекта при ОКР можно достигнуть с помощью трициклических антидепрессантов и, главным образом, кломипрамина (анафранил) (Lopes-Ibor J.J., 1969; Beaumont G., 1973; Escobar H., Landblom R., 1976; Katz R.J. с соавт., 1990 и др.). Помимо кломипрамина, с определенным успехом применялись имипрамин, амитриптилин, доксепин и дезипрамин (Ananth J. с соавт., 1981; Jenike М. А., 1989 и др.). Большинство этих исследований было выполнено на небольшом контингенте больных и без надлежащего контроля. Терапевтический эффект этих антидепрессантов был малопредсказуемым и не был четко связан с депрессивной симптоматикой.
Первую успешную попытку применения кломипрамина с внутривенным введением при навязчивостях еще в 1969 году предпринял J.J. Lopes-Ibor. При этом у 13 из 16 больных в течение 2-5 дней отмечалась редукция обсессивно-фобической симптоматики. Эти данные в последующем были подтверждены в многочисленных исследованиях, в том числе плацебо-контролируемых. Подробные обзоры этих работ были сделаны М. A. Jenike (1989) и S. Montgomery (1993, 1999). Общая эффективность при применении кломипрамина внутрь или парентерально варьировалась от 40 до 80%. Нужно упомянуть, что эффект плацебо при ОКР в отличие от депрессии составляет только 5% (Katz R.J. с соавт., 1990). В среднем терапевтические дозы составляли от 75 до 300 мг/сут и устойчивый эффект при пероральном приеме развивался в течение 4-6 недель терапии, хотя у многих больных значительное улучшение наступало уже в первые 2 недели лечения, а при внутривенном введении — в первые дни. Достигнутый эффект, как правило, требовал проведения поддерживающей терапии, результаты которой при применении умеренных доз препарата (75-150 мг/сут) в течение 1-4 лет (Thoren Р. с соавт., 1980; Katz R.J. с соавт., 1990 и др.) были весьма хорошими. У 90% больных при отмене кломипрамина развивалось обострение симптоматики.
Особый интерес представляют сравнительные исследования кломипрамина с другими трициклическими антидепрессантами: амитриптилином (Ananth с соавт., 1981), имипрамином (Volavka J. с соавт., 1985), доксепином (Ananth J., Van den StreenN., 1977), в которых было убедительно показано существенное преимущество кломипрамина в отношении купирования идеаторных навязчивостей (обсессий), ритуалов (компульсий) и фобической симптоматики. В отношении редукции депрессивной и тревожной симптоматики были получены менее очевидные результаты, хотя и здесь кломипрамин несколько превосходил все другие трициклические антидепрессанты.
Большинство исследователей сходятся во мнении, что кломипрамин обладает выраженным самостоятельным антиобсессивным эффектом, не связанным прямо с его не менее мощным тимоаналептическим действием. Другими словами, хотя присутствие депрессивных или дисфорических переживаний в рамках обсессивно-компульсивного синдрома нередко увеличивает глобальную эффективность кломипрамина, их отсутствие еще не означает, что препарат будет неэффективным.
Особое место кломипрамина среди других трициклических антидепрессантов предопределило развитие серотонинергической гипотезы патогенеза ОКР, поскольку кломипрамин в 5 раз сильнее блокирует реаптейк серотонина, чем, например, дезипрамин. В исследовании Р. Thoren с соавт. (1980), в частности, было показано, что клинический эффект кломипрамина сильно коррелирует с повышенным содержанием 5-оксииндолилуксусной кислоты (5-ОИУК) (основной продукт метаболизма серотонина) в спинно-мозговой жидкости, которое снижается после курса терапии. Это может свидетельствовать об угнетении центральной серотонинергической активности.
Специальное изучение применения кломипрамина у больных с обсессивно-фобическими нарушениями в нашей клинике показало, что нозологическая принадлежность очерченного синдрома навязчивостей существенно не влияет на эффективность препарата. Кломипрамин в одинаковой мере обнаружил способность редуцировать навязчивости (в том числе, ритуальные) как при депрессии, так и в рамках невроза или при неврозоподобной шизофрении. Лучшие результаты наблюдались при ограниченном круге навязчивостей или моноритуалах (например, при частом мытье рук). При генерализованном ОКР (например, при совершении множественных очищающих ритуальных действий, доминировании идеаторных навязчивостей, граничащих со сверхценным представлением, а у больных шизофренией с интерпретативными бредовыми идеями) эффективность кломипрамина была существенно ниже.
Методика применения кломипрамина при ОКР несколько отличается от его применения при депрессиях и панических атаках. Начальные дозы составляют 25-50 мг/сут, их постепенно наращивают на 25-50 мг в день. Терапевтический эффект обычно развивается на дозах 225-300 мг/сут. При выраженных навязчивостях с длительным течением можно сразу начинать с внутривенного капельного введения 25-50 мг/сут с постепенным (за 5-10 дней) доведением дозы до 200-250 мг/сут (методика проведения капельных инфузий не отличается от таковой при депрессиях). При резистентных навязчивостях переход к внутривенному введению кломипрамина часто оказывается более эффективным, чем пероральный прием (Koran L. М., с соавт 1997; Fallon В. А. с соавт., 1998). Курс терапии составляет 2 недели. Чаще внутривенные инфузии кломипрамина (100-125 мг/сут) комбинируют с приемом препарата внутрь (100-200 мг/сут). При этом в первые часы после инфузии необходимо следить за артериальным давлением. С целью профилактики ортостатического коллапса больной должен находиться в горизонтальном положении еще в течение часа после окончания инфузионной терапии кломипрамином. При достижении эффекта, который обычно наступает в течение первых двух недель терапии, переходят на пероральный прием препаратов, который следует продолжать еще в течение 4-6 месяцев, а при тяжелых, вызывающих социальную дезадаптацию навязчивостях, и более длительный срок. При этом от клинициста требуется, во-первых, добиться редукции или исчезновения навязчивостей и, во-вторых, определить минимальную дозу кломипрамина, которая будет достаточна для контроля за обсессивной симптоматикой, но не будет вызывать дезадаптирующих побочных эффектов. В случае решения об отмене терапии дозу также следует снижать крайне постепенно, так как резкое прекращение приема препарата, как правило, приводит к возобновлению обсессивно-компульсивных переживаний и может вызвать синдром „отмены».
Препарат в целом хорошо переносится больными и не вызывает экзацербации тревожной симптоматики, как это отмечается в случае его применения при панических атаках. К основным побочным эффектам следует отнести антихолинергические явления (нарушения аккомодации, запоры, задержка мочи, сухость во рту, спутанность), ортостатическую гипотензию, реже кардиотоксические эффекты (необходим ЭКГ мониторинг) и снижение порога судорожной активности.
Таким образом, по антиобсессивному эффекту кломипрамин не только превосходит все другие трициклические антидепрессанты и ниаламид, но и традиционно рекомендовавшиеся ранее в этих целях бензодиазепиновые транквилизаторы и малые нейролептики. Кломипрамин является, пожалуй, оптимальным препаратом для лечения ОКР. Это касается как его воздействия на собственно обсессивно-компульсивное ядро расстройства, так и на симптоматику тревоги и депрессии, сопутствующую основным переживаниям.
Особый интерес для развития серотонинергической гипотезы патогенеза ОКР представляет эффективность селективных ингибиторов обратного захвата серотонина (СИОЗС). Дело в том, что кломипрамин и особенно основной его метаболит — дезметилкломи-прамин обладают также сильной способностью блокировать реаптейк норадреналина. К настоящему времени при ОКР, в том числе в рандомизированных плацебо-контролируемых исследованиях (РКИ), хорошо изучено действие флувоксамина (Greist J.H., 1990; Jenike М. А., с соавт., 1990; Tamimi R., с соавт., 1991; GoodmanW. К. с соавт., 1992,1996; Граненов Г. М., Мосолов С. Н., 2003; Wakatani Е., с соавт., 2005 и др.), флуоксетина (Pigott Т. А. с соавт., 1990; Hantouche Е., 1993; Montgomery S. с соавт., 1993; Tollefson G. D. соавт., 1994; Jenike М. А., 1997; Zitterl W. с соавт., 1999 и др.), сертра-лина (Chouinard G. с соавт., 1990; Greist J. с соавт., 1995; Bisserbe J. С. с соавт., 1997; Kronig М. с соавт., 1999; Koran L. с соавт., 2002 и др.), пароксетина (ZoharJ., Judge R., 1994, 1996; Wheadon D.A. с соавт., 1995; Steiner M. с соавт., 1995; Hollander E. С соавт., 2003; Kamijima K. С соавт., 2004; Stein D.J. с соавт., 2007 и др.) и циталопрама (Stein D.J., с соавт., 1996; Montgomery S. А. с соавт., 2001; Marazziti D., с соавт., 2001 и др.). Все эти препараты оказались достаточно эффективными (т. е. превосходили плацебо) как в отношении редукции идеаторных навязчивостей, так и ритуальных действий, независимо от того, насколько выраженной была сопутствующая депрессивная симптоматика, а также оказывали противорецидивный эффект при длительной терапии. Эсциталопрам не только превосходил по эффективности плацебо, но и препарат сравнения пароксетин (Stein D.J. с соавт., 2007), а также обладал лучшим по сравнению с плацебо противорецидивным действием (Fineberg N. А. с соавт., 2007).
Прямые двойные слепые сравнительные исследования кломипрамина и СИОЗС, также как и сравнение отдельных СИОЗС между собой, а также несколько мета-анализов этих работ не выявили существенной разницы между препаратами (Greist J. с соавт., 1995; Stein D., с соавт., 1995; Milanfranchi А. С соавт., 1997; Lopez-IborJ. с соавт., 1996; Janicak Ph. G. с соавт., 1997; Montgomery S., Zohar J., 1999; Pigott T. A., Seay S. M., 1999; Zohar J. с соавт., 2000; Mundo E. С соавт., 2000 и др.), хотя величина эффекта была несколько больше у кломипрамина. Это отчасти объясняется тем, что хотя кломипрамин не является селективным ингибитором реаптейка серотонина, по мощности своего серотонинергического воздействия он в 2 раза превосходит флувоксамин и в 4 раза флуоксетин (Мосолов С. Н., 1995).
Эффект СИОЗС развивается достаточно быстро (уже на 2-4-й неделе терапии) и постепенно усиливается к 8-12-й неделям. При этом первоначальное улучшение высоко коррелирует с общей курсовой эффективностью антидепрессанта. Терапевтические дозы препаратов близки к максимальным и в среднем выше, чем при лечении депрессий. Для флувоксамина они составляют 150-300 мг/сут, флуоксетина — 40-80 мг/сут, сертралина — 150-250 мг/сут, пароксетина — 40-60 мг/сут, и циталопрама — 40-60 мг/сут, эсциталопрама — 10-20 мг/сут (Jefferson J.W. с соавт., 1996; March J.S. с соавт., 1997; Zohar J. с соавт., 2002). При этом у некоторых препаратов была обнаружена прямая корреляция между дозой и эффективностью (Wheadon D. А. с соавт., 1995; Montgomery S. А. с соавт., 2001). Эти данные согласуются с результатами экспериментальных исследований, показывающих, что десенсибилизация орбитофронтальных серотониновых рецепторов становится заметной только после длительного применения высоких доз СИОЗС (El Mansari М. с соавт., 1995).
Наши собственные исследования подтвердили существенные преимущества серотонинергических антидепрессантов (кломипрамина и флувоксамина) по сравнению с норадренергическими антидепрессантами (дезипрамин) в отношении редукции обсессивно-фобической симптоматики, независимо от диагностических рамок (см. рис. 3). При этом эффект, т.е. не менее чем 25 % редукция симптоматики по шкале Y-BOCS, через 2 месяца терапии наблюдался у 50-70% больных (см. рис. 4). Значимые различия наблюдались уже через 2-4 недели терапии, они прогрессивно нарастали вплоть до 12-й недели лечения. Эффект кломипрамина развивался более быстро, и в первые недели терапии он несколько превосходил флувоксамин как по темпу редукции симптоматики, так и по числу респондеров (см. рис. 3 и 4). Эти различия практически исчезали, начиная с 4-6-й недели лечения, и через 3 месяца кломипрамин уже несколько уступал флувоксамину.
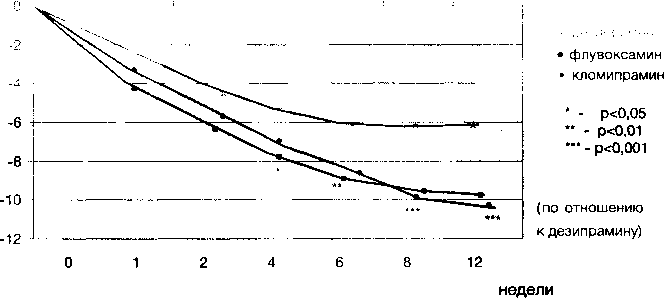
Рис. 3 Сравнительная эффективность кломипрамина, дезипрамина и флувоксамина при ОКР (редукция симптоматики по шкале Y-BOCS)
Редукция баллов по шкале Y-BOCS
Продолжительность терапии СИОЗС в среднем составляет около 3 месяцев, но в некоторых исследованиях была более двух лет (Montgomery S. А., 1997). В большинстве случаев в течение года после отмены лечения обсессивно-компульсивная симптоматика возобновилась, хотя у ряда больных удалось наблюдать и более устойчивые ремиссии (Hantouche Е., 1993, Montgomery S. А., 1997), особенно при их подкреплении адекватной психотерапией. При проведении поддерживающей терапии СИОЗС имеют несомненное преимущество перед кломипрамином, так как обладают значительно лучшей переносимостью и субъективно лучше воспринимаются больными. В настоящее время общепринятым считается необходимость проведения как минимум годовой терапии серотонинергическими антидепрессантами (Jefferson J.W. с соавт., 1996; March J.S. с соавт., 1997; Zohar J. с соавт., 2002 и др.). В случае принятия решения об отмене эффективной профилактической терапии делать это нужно крайне постепенно, уменьшая дозу на 20-30 % каждые 2-3 месяца.

Рис. 4. Число респондеров (> 25 % редукции симптоматики по шкале Y-BOCS) в динамике терапии кпомипрамином, дезипрамином и флувоксамином
Среди других антидепрессантов миртазапин в дозах 30-60 мг/сут превосходил плацебо в двойной слепой период отмены после открытой фазы исследования (Koran L. М. с соав., 2005). Добавление миртазапина к циталопраму не приводило к увеличению эффективности при сравнении с добавлением плацебо, но было связано с более быстрым началом действия (Pallanti S. с соавт., 2004). В двойном слепом плацебо контролируемым исследовании венлафаксин (селективный ингибитор обратного захвата серотонина и норадреналина) не обнаружил эффекта при ОКР (Yaryura-Tobias J. A., Neziroglu F.A., 1996), однако объем выборки, доза и продолжительность исследования были недостаточными. В двойном слепом перекрестном исследовании с пароксетином оба препарата были одинаково эффективны (Denys D. С соавт., 2003).
Психофармакотерапевтический анализ, т.е. избирательная эффективность серотонинергических антидепрессантов при ОКР, позволяет сделать, по крайней мере, два важных вывода. Во-первых, как диагностическая категория ОКР должно быть обособлено как от тревожных расстройств, так и от депрессий. И в этом смысле МКБ-10 является более совершенной классификацией по сравнению с DSM-IV. При тревожных расстройствах, например, при панических атаках, помогают многие ТЦА, тогда как при навязчивостях только кломипрамин. Тревожно-фобическая симптоматика при ОКР, несомненно, является составной частью целостного синдрома, поскольку полностью редуцируется только под влиянием ингибиторов реаптейка серотонина, но не под влиянием бензодиазепиновых транквилизаторов или других анксиолитических средств. Вторым важным выводом является очевидная заинтересованность (недостаточность функции) серотонинергических центральных структур. Именно прямым повышением содержания серотонина в синаптической щели можно, по-видимому, объяснить более быстрый по сравнению с депрессией и достаточно избирательный эффект пресинаптических ингибиторов захвата серотонина.
Таким образом, патогенетическим подходом к терапии ОКР в настоящее время, по-видимому, является усиление серотонинергической нейропередачи путем применения ингибиторов реаптейка серотонина (кломипрамин, СИОЗС). Вследствие опосредованного усиления дофаминергической передачи через 5-НТ2А ,1-ауторецепторы в некоторых случаях эффективно также присоединение дофаминоблокаторов — антипсихотичеких средств (пимозид, галоперидол, рисперидон и др.) И, наконец, у тяжелых, резистентных к фармакотерапии больных в 30 %-50 % случаях помогает хирургическое вмешательство — стереотаксическая цингулотомия, хотя развитие серьезных осложнений, в том числе судорожного синдрома, значительно ограничивает ее применение (см. рис. 5).
В случае отсутствия или недостаточности эффекта в течение 2-3 месяцев лечения следует прежде всего еще раз оценить правильность диагностики и соблюдение больным режима терапии. Если в состоянии больного имеется определенная положительная динамика, то, по-видимому, целесообразно продолжить терапию в тех же или несколько больших дозах еще в течение 2-3 месяцев.
При отсутствии эффекта от одного препарата, что наблюдается примерно у 30-50% больных (Montgomery S.A., 1993; Stein D.J., с соавт., 2001 и др.), в ряде случаев можно рассчитывать на эффект других серотонинергических антидепрессантов, поскольку несмотря на общий механизм действия эти соединения различаются между собой в структурном отношении и могут действовать на разные типы серотониновых рецепторов (Greist Т.Н. с соавт., 1995; Pigott Т.А., SeayS.M., 1999 и др.).
С целью усиления серотонинергического действия антидепрессантов можно попробовать присоединение солей лития или вальпроевой кислоты, а также топирамата, что особенно эффективно при комор-бидном биполярном расстройстве, а также при нарушении контроля импульсных влечений. (Rasmussen S.A., 1984; Greist J. М., 1990; Pigott Т. А., с соавт., 1991; McDougle C.J. с соавт., 1997; Hollander Т., Dell’osso D., 2006; Van Ameringen М. с соавт., 2006 и др.) Литий, как известно, способствует выделению серотонина в синаптических окончаниях. За счет этого усиливается нейротрансмиссия, и можно рассчитывать на определенное повышение эффективности. Для этой цели обычно применяют 600-900 мг карбоната лития в сутки. Нужно, однако, опасаться развития „серотонинового“ неврологического синдрома. По этим же соображениям следует избегать совместного применения серотонинергических препаратов с L-триптофаном, фенфлурамином или ингибиторами МАО, хотя в особо тяжелых и терапевтически резистентных случаях именно такие комбинации могут оказаться эффективными.
Как известно, L-триптофан является естественным предшественником серотонина и его дополнительное введение в дозе 6-8 г в сутки особенно оправдано при снижении синтеза или истощении запасов серотонина, например, вследствие длительного применения серотонинергических антидепрессантов. Терапевтический эффект обычно становится очевиден через 1-2 недели терапии, однако у части больных при продолжении лечения он склонен истощаться (Rasmussen S. А., 1984; Beier R, Bergeron R., 1996). Действие L-триптофана может быть усилено назначением ингибиторов печеночной пирролазы (разрушающий фермент) — никотиновой кислоты или никотинамида (Chouinard G. с соавт., 1977), а также пиридок-сина (витамин В6) и аскорбиновой кислоты (витамин С), которые также принимают участие в синтезе серотонина. Помимо „серо-тонинового“ синдрома, при применении L-триптофана возможно развитие эозинофилии, миалгий и иммунных нарушений.
Фенфлурамин и ингибиторы МАО усиливают высвобождение серотонина нервными окончаниями и неэффективны после длительного применения СИОЗС (Hollander Е. с соавт., 1990). Фенфлурамин в последнее время не применяется вследствие потенциально высокого риска сердечной токсичности.
Еще одной возможностью в случае отсутствия эффекта и особенно при развитии навязчивостей в рамках неврозоподобной шизофрении или коморбидности с синдромом Туретта и другими моторными нарушениями является присоединение нейролептиков (преимущественно пимозид или галоперидол) в индивидуально подобранных дозах с учетом переносимости (Delgado Р. L. с соавт., 1990; Hantouche Е., 1993; McDougle C.J. с соавт., 1994; Sasson Y. с соавт., 1997; Колюцкая Е. В., 1999). Делать это, однако, следует с осторожностью, так как экстрапирамидная побочная симптоматика может усилить навязчивости. Поэтому в последнее время предпочтение отдается атипичным антипсихотикам. В РКИ показана более высокая эффективность по сравнению с плацебо присоединения к СИОЗС рисперидона (Ravizza L. с соавт., 1996; Me Dougle C.J. с соавт., 2000; Hollander Е. с соавт., 2003; Li X. с соавт., 2005; Erregovesi S. с соавт., 2005), оланзапина (Bogetto Е с соавт., 2000; Bystrisky А. с соавт., 2004; ShapiraN.A. с соавт., 2004) и кветиапина (Denys D. С соавт., 2004; Fineberg N. А. с соавт., 2005, 2006). Имеются также данные открытых исследований по эффективности присоединения арипипразола (Connor К. М. с соавт., 2005; da Rocha Е Е, Corea Н., 2007).
Сравнение рисперидона и кветиапина в качестве препаратов аугментации СИОЗС при ОКР не обнаружило различия в их эффективности (Maina G. С соавт., 2008). В целом, мета-анализы исследований по повышению эффективности СИОЗС атипичными антипсихо-тиками показали положительный баланс, особенно в отношении рисперидона (Bloch M.N. с соавт., 2006; Skapinakis Р. с соавт., 2007).
Хотя собственно антиобсессивный эффект в спектре действия анксиолитиков (транквилизаторов) отсутствует, комплексное назначение этих соединений с антидепрессантами при курации резистентных больных вполне целесообразно, поскольку они смягчают тревожный компонент навязчивостей и особенно эффективны при сочетании с другими тревожными расстройствами. Для этих целей лучше применять клоназепам в дозе 1-4 мг/сут (Hewlett W. А. с соавт., 1992; Crokett В. А. с соавт., 2004) или буспирон в дозе 20-40 мг/сут, являющийся агонистом 5 НТ1А-серотониновых рецепторов и обнаруживший, по предварительным данным, способность усиливать действие флуоксетина у резистентных больных с навязчивостями (Markovitz А. с соавт., 1989; Pato М.Т. с соавт., 1991; McDougle C.J. с соавт., 1993; Grady Т., с соавт., 1993). Однако слепое плацебо контролируемое исследование Pigott Т. А. с соавт. (1992) не обнаружило усиления действия кломипрамина. Буспирон хорошо переносится, однако не следует сочетать его с ингибиторами МАО из-за возможности повышения артериального давления, а также галоперидолом из-за увеличения его концентрации в плазме крови. В одном РКИ присоединение пиндолола к пароксетину оказалось успешным (Dannon P.N. с соавт., 2000), но добавление пиндолола к флувоксамину не оказывало никакого эффекта (Mundo Е. с соавт., 1998).
У некоторых больных за счет интенсификации процесса снижения плотности и чувствительности постсинаптических рецепторов (запуска феномена фармакологической адаптации рецепторов) может оказаться эффективным присоединение тразодона или миртазанина, который является антагонистом 5 НТ2-рецепторов (Hermesh Н. с соавт., 1990; Pigott Т. А. с соавт., 1992; Pallanti S. с соавт., 2004). Препараты оказывают также отчетливый самостоятельный анксиолитический эффект. В открытых исследованиях показана эффективность антиандрогенного препарата — ципротерона (Casas М. с соавт., 1986), антагониста глутаминовых рецепторов — рилузола (Coric V. с соавт., 2005), антагониста NMDA рецепторов мемантина (Poyurovsky М. С соавт., 2005; Pasquini М., Biendi М., 2006;), N-ацетилцистеина (Lafleur D. L. с соавт.,2006), гонадотропинрелизинг гормона аналога трипторелина (Eriksson Т., 2007). Современные рекомендации по лекарственной терапии ОКР на основе анализа данных доказательных клинических исследований приведены в таблице 1.
При тяжелых, некупирующихся фармакотерапией навязчивостях прибегают к нелекарственным методам терапии: электросудорожной (ЭСТ), транскраниальной магнитной стимуляции (ТМС), глубокой стимуляции мозга (ГСМ), стереотаксической передней капсулотомии или цингулотомии (Mindus R, Jenike М.А., 1992; Husain М. С соавт., 1993; Maletzky В. с соавт., 1994; Greenberg B.D. с соавт., 1997; Jenike М. А., 1998; Alonso Р. с соавт., 2001; Мосолов С.Н., 2002; Abelson J. L. с соавт., 2005; Mantovani А. с соавт., 2006; Greenberg В. D. с соавт., 2006).
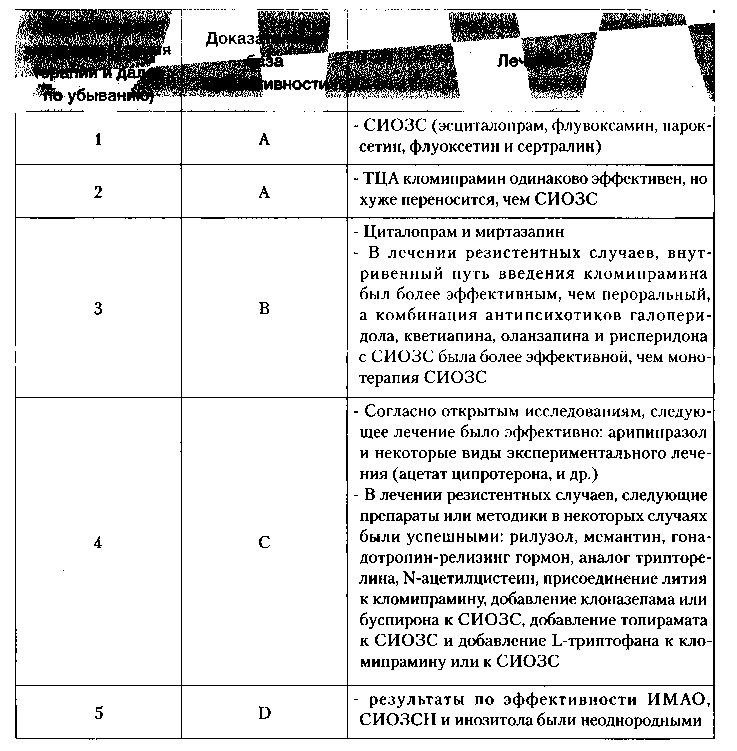
Таблица 1. Рекомендации по лекарственной терапии ОКР на основе анализа доказательных клинических исследований (адаптировано из Bandelow В. с соавт., 2008) Примечание. А — наиболее достоверные данные, доказательства получены на основании нескольких рандомизированных двойных слепых плацебо контролируемых исследований и/или в мета-анализе нескольких РКИ; В — ограниченные положительные доказательства, полученные хотя бы в одном РКИ; С -Доказательства из неконтролируемых исследований или исследований с описанием серии случаев/мнения экспертов; D — неоднородные результаты, положительные РКИ сопровождаются приблизительно равным количеством отрицательных исследований.
На любом этапе лечения ОКР крайне важно сочетание биологических методов лечения с психотерапией, которая должна проводится интенсивно и длительно. Наиболее эффективной является поведенческая психотерапия (постепенное увеличение экспозиции триггерных ситуаций с целью десенсибилизации). В отличие от медикаментозной терапии, после отмены которой наблюдаются частые случаи обострения симптоматики ОКР достигаемый поведенческой психотерапией эффект сохранялся в течение нескольких месяцев и даже лет. Компульсии, как правило, лучше поддаются психотерапии, чем обсессии. Общая эффективность поведенческой психотерапии примерно сопоставима с фармакотерапией и составляет 50-60%, однако, к сожалению, многие больные отказываются от участия в ней из-за страха усиления тревоги. Применяются также групповая, рациональная, психообразовательная (обучение больного отвлекаться на другие стимулы, облегчающие тревогу), аверсивная (применение болезненных стимулов при появлении навязчивостей), когнитивная, семейная и некоторые другие методы психотерапии (Zohar J., Insel Т. R., 1987; Jenike М. А. с соавт., 1990; Abramowitz J.S., 1997; Stein D.J. с соавт., 2001 и др.). Необходимо проведение и различных социо-реабилитационных мероприятий.