В статье представлены результаты исследования, в котором изучалось влияние циклической ТМС левой дорсолатеральной префронтальной коры на когнитивные функции при лечении депрессии у больных шизофренией. Исследование показало, что циклическая ТМС по своим тимоаналептическим свойствам не уступает традиционным методам психофармакотерапии этих состояний, а также обладает стимулирующим действием на когнитивную сферу.
В наибольшей степени при ТМС улучшались исполнительские функции и переключаемость внимания, при этом их быстрое улучшение совпадало с положительным ответом на терапию. Число респондеров в группе ТМС составило 62,5% против 52,9% в контрольной группе. Также ТМС обнаружила высокую эффективность (64,5% респондеров) в группе больных с резистентными депрессиями в рамках шизофрении. К особенностям действия ТМС у данной категории больных можно отнести хорошую переносимость, более быстрое развитие антидепрессивного эффекта и более выраженную редукцию негативных симптомов по сравнению с контрольной группой.
Актуальность проблемы депрессий при шизофрении определяется, прежде всего, их высокой распространенностью (Martin R. L. et al., 1985), ухудшением прогноза заболевания в целом (Birchwood М. et al., 1993; Johnson D. A. W., 1988; Mandel M.R. et al., 1982; Roy A. et al., 1983), а также снижением качества жизни у этой категории больных (Norholm V. et al., 2006). Недостаточная эффективность психофармакотерапии при этих состояниях определяет интерес к нелекарственным методам лечения, таким как ТМС (Мосолов С. Н., 1995).
Эта методика позволяет локально стимулировать определенные участки коры головного мозга, в частности левую дорсолатеральную префронтальную кору (ЛДЛПК), с дисфункцией которой связывают негативные, депрессивные и когнитивные нарушения у больных шизофренией (Wolf С. et al., 2011; Molina V. et al., 2009; Ettinger U. et al, 2011). Несмотря на более чем 20-летнюю историю метода и широкое его применение в ряде стран (Канада, Израиль и др.) для лечения депрессий, данные об использовании ТМС у больных шизофренией довольно ограничены (Holtzheimer Р.Е. et al., 2001). Учитывая положительное влияние ТМС на когнитивную сферу у больных резистентными депрессиями (Пуговкина О.Д. с соавт., 2006), представляет собой интерес выяснить, имеются ли схожие эффекты при использовании данной методики у больных шизофренией с депрессивной симптоматикой.
Дезорганизованное мышление при шизофрении выражается в бедности речи, нарушениях внимания, алогичности, ассоциативной нечеткости и неизбежно отражается в результатах нейропсихологического тестирования (Иванов М. В. с соавт., 2008). В тоже время проявления депрессии с присущими ей анергией, апатией и психомоторной заторможенностью также накладывают отпечаток на когнитивное функционирование больных шизофренией. Учитывая то, что в исследовании принимали участие пациенты, страдающие шизофренией с преобладанием негативной симптоматики и наличием депрессии, когнитивные тесты являлись важным инструментом в оценке терапевтической динамики, отражая изменения основных психопатологических синдромов в процессе лечения. Целью нашего исследования являлось изучение когнитивных функций у больных шизофренией с депрессивной симптоматикой во время проведения курса ТМС и адекватной психофармакотерапии. Другой задачей являлось установление взаимосвязи динамики когнитивных показателей с изменениями в психическом состоянии больных во время лечения, а также поиск прогностических факторов успешной терапии.
Материалы и методы. В исследование было включено 97 больных шизофренией (МКБ-10) в возрасте от 17 до 65 лет. Все больные были вне обострения психотической симптоматики и были оценены не менее чем в 6 баллов по Шкале депрессии при шизофрении Калгари (CDSS) (Addington D. et al., 1992), что свидетельствовало о наличии очерченной депрессии. У всех пациентов негативная симптоматика преобладала над позитивной (средний композитный индекс PANSS составлял -11).
Все больные находились на стабильной антипсихотической терапии за 2 недели до начала и на протяжении всего исследования. Большинство пациентов получало атипичные нейролептики (85,6%). У больных не отмечалось клинически значимой экстрапирамидной симптоматики. Исходя из целей и задач исследования больные были разделены на 3 терапевтические группы. Больным первой группы проводился курс ТМС левой ДЛПК на аппарате «Нейро-МС» (Нейрософт, Иваново) с амплитудой равной моторному порогу, частотой 15 Гц, трейнами по 6 секунд и интервалами между трейнами в 60 секунд. Число трейнов за процедуру составляло 20 (1800 импульсов). Процедуры проводились ежедневно с перерывами на выходные, число процедур за курс составляло 15-20. Пациентам этой группы не назначались антидепрессанты на протяжении всего исследования.
Больным второй группы проводилась адекватная психофармакотерапия, заключавшаяся в добавлении к схеме лечения антидепрессанта, или замене уже имевшегося антидепрессанта на препарат с другим механизмом действия. Выбор препарата и подбор дозировки был индивидуальным. Эта группа являлась активным контролем для первой группы. Распределение в первые две группы было рандомизированным. Третья группа состояла из терапевтически-резистентных больных, получавших комбинированную (нейролептик в сочетании с антидепрессантом), но неэффективную в отношении депрессивной симптоматики терапию на протяжении не менее 3-4 недель до начала и на протяжении всего исследования. Больным этой группы проводился курс ТМС по описанной выше методике.
Группы были сопоставимы по основным демографическим и психометрическим показателям. Все пациенты еженедельно оценивались по CDSS, шкале позитивных и негативных синдромов (PANSS), а также при помощи батареи когнитивных тестов. В исследовании оценивались наиболее важные когнитивные функции, такие как внимание, память, ассоциативная продуктивность. Показатели внимания оценивались по тестам «Кодировка» (Wechsler D., 1955) и «Счет с переключением» (Савина Т. Д., 1982), мнестические функции по тесту Бентона (Benton А., 1960) и тесту «10 слов» (Лурия А.Р., 1969).
Вербальная ассоциативная продуктивность исследовалась по тесту «Беглость речевых ответов» (Lezak М. D., 1995). Эффективность терапии оценивалась через 3 недели после ее начала, что соответствовало окончанию курса ТМС. Критерием эффективности являлась 50% редукция показателей по шкале CDSS. С целью статистической обработки данных использовалась программа STATISTICA 6.0. Для оценки статистической достоверности изменений показателей внутри групп применялся тест согласованных пар Уилкоксона. Для определения достоверности межгрупповых различий показателей использовался U критерий Манна-Уитни.
Результаты. Число респондеров с 50% редукцией показателей по CDSS составило в 1-й группе (АП+ТМС) 20 больных (62,5%), во 2-й группе (АП+АД) 18 больных (52,9%), в 3-й группе (АП+ АД+ТМС) 20 больных (64,5%). Редукция суммарного балла по CDSS к концу 3-й недели терапии составила 50,6% (р<0,05), 47,4% (р<0,05), 55,2% (р<0,05) соответственно по группам. Также во всех группах снизился общий балл по негативной подшкале PANSS. Максимальная редукция показателей по этой подшкале была в 3-й группе (АП+АД+ТМС) и составила 21,3% (р<0,05) к окончанию курса ТМС. В 1-й группе (АП+ТМС) этот показатель был равен 15,5% (р<0,05), во 2-й группе (АП+АД) — всего 5,8% (р<0,05). Изменения по позитивной подшкале PANSS были статистически значимыми только в 1-й группе (АП+ТМС), однако степень редукции продуктивной симптоматики в процессе ТМС была невелика и составляла 13,7% (р<0,05) к окончанию курса.
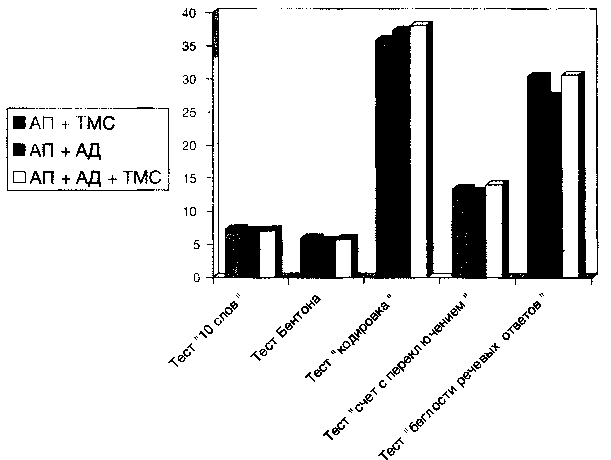
Как видно из приведенного ниже рисунка 1, значимых различий по результатам когнитивных тестов между терапевтическими группами на момент начала исследования не было.
Следует отметить, что показатели по большинству когнитивных тестов в исследуемой когорте пациентов были ниже, чем у больных резистентными депрессиями в работе Пуговкиной О. Д. (Пуговкина О.Д. с соавт., 2006), что свидетельствует о несомненной роли процессуального дефекта в формировании когнитивного дефицита при депрессиях в рамках шизофрении. Особенностью при выполнении когнитивных тестов больными шизофренией была сниженная мотивация и незаинтересованность в конечном результате тестирования. Пациенты часто нуждались в подбадривании и поощрении при выполнении заданий, в противном случае могли отказаться от продолжения работы в самом начале теста, сославшись на усталость или незнание правильного ответа. Также отмечались сложности в понимании условий тестов, что требовало повторных объяснений заданий.
Обращала на себя внимание некритичность больных к своим ошибкам и стереотипное их повторение, даже при указании на них исследователем. Указанные особенности тем сильнее были выражены, чем больше был удельный вес негативных расстройств в состоянии больных. Корреляционный анализ показал, статистически достоверную обратную связь выраженности негативной симптоматики и результативности по всем когнитивным тестам. Наиболее значимые корреляции негативной подшкалы PANSS прослеживались с показателями тестов «Кодировка» и «Счет с переключением». Именно эти тесты отражают внимание и исполнительские функции, которые в наибольшей степени страдают у больных шизофренией. Обращает на себя внимание то, что выраженность депрессии не имела значимых корреляций с результатами ни одного из использованных когнитивных тестов.
По-видимому, депрессивная симптоматика не вносила существенного вклада в имевшийся у исследуемых больных когнитивный дефицит. Последний был больше связан с негативной симптоматикой, хотя и не исключается его первичная природа. В приведенной ниже таблице представлены коэффициенты корреляции Спирмена между основными психометрическим показателями (Шкала CDSS, Шкала PANSS и её подшкалы) и показателями когнитивных тестов на момент включения больных в исследование.
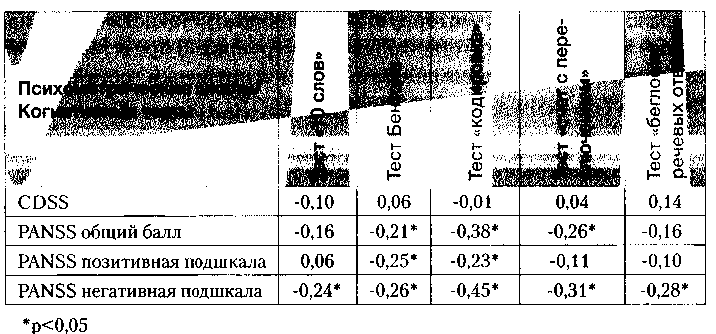
Таблица 1. Корреляции Спирмена между основными психометрическими показателями и результатами когнитивных тестов
Следует отметить, что показатели ни одного из применявшихся когнитивных тестов не коррелировали в значимой мере ни с возрастом пациентов, ни с длительностью течения заболевания. Таким образом, когнитивное функционирование исследуемых больных в большей степени зависело от текущего психического статуса, а именно от выраженности негативных расстройств.
Анализ терапевтической динамики когнитивных функций показал наибольший прирост показателей по тестам «кодировка” и «счет с переключением», т. е. по тем тестам, которые в наибольшей степени коррелировали с изначальной выраженностью негативных расстройств. Следует отметить, что в группах, в которых проводилась ТМС, улучшение по этим тестам было наибольшим. Прирост показателей по тесту «кодировка» в 1-й группе (АП+ТМС) и в 3-й группе (АП+АД+ТМС) составил 20,3% и 17,5% соответственно, и только 11,4% в контрольной группе (АП+АД). В отношении теста «счет с переключением» прослеживались аналогичные тенденции, в контрольной группе прирост показателей был наименьшим — 14,0%, против 22,3% и 23,5% в 1-й (АП+ТМС) и 3-й (АП+АД+ТМС) группах.
Внутригрупповые изменения показателей по этим тестам были статистически достоверными во всех группах (р<0,05), однако межгрупповые различия можно было отметить лишь на уровне тенденций. По тестам «10 слов» (отражает вербальную память) и «тест беглости речевых ответов» (отражает ассоциативные процессы) изменения показателей внутри групп были минимальными, а по тесту Бентона (отражает зрительно-моторную координацию) статистически значимые изменения отсутствовали во всех группах. В представленной ниже таблице приведены показатели по когнитивным тестам в терапевтических группах до и после лечения.
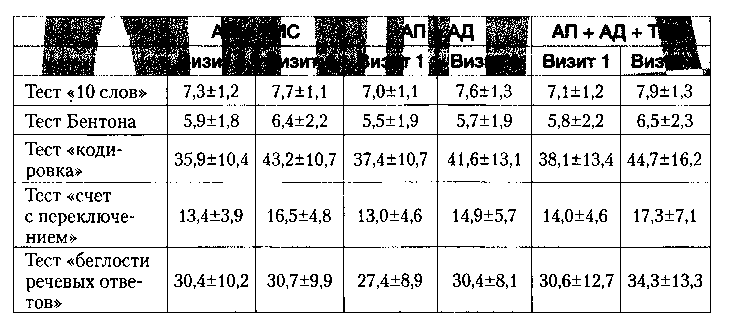
Таблица 2. Результаты когнитивных тестов по группам на момент начала исследования и к концу 3-й недели терапии (в баллах)
У большинства пациентов достигнутые изменения когнитивных функций были достаточно стойкими. Заметное ухудшение когнитивных показателей в период последующего двухнедельного наблюдения наблюдалось лишь у 3-х больных (9,4%) в 1-й группе (АП+ТМС) и у 2-х больных (6,6%) 3-й группы (АП+АД+ТМС). В наибольшей степени обратной динамике у этих больных были подвержены показатели тестов «кодировка» и «счет с переключением», т. е. тех же, которые в первую очередь и улучшались. Это, по всей видимости, связано с возможным исчерпыванием стимулирующего действия ТМС на исполнительские функции и переключаемость внимания после окончания курса. Стоит отметить, что, несмотря на обратную динамику, результаты тестов все же превосходили фоновые. Ухудшение было отчетливее выражено в 1-й группе (АП+ТМС), причем у двух больных оно совпало с частичным возвратом депрессивной симптоматики.
В контрольной группе показатели когнитивных тестов в период последующего наблюдения не ухудшались.
Ниже будет приведено описание динамики когнитивных функций по терапевтическим группам в отдельности.
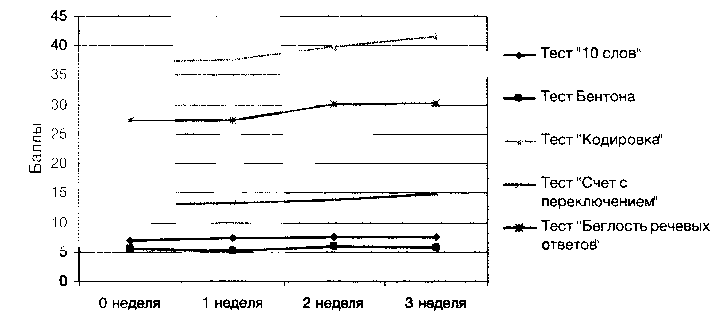
На представленной диаграмме показаны результаты когнитивных тестов в 1-й группе (АП+ТМС) при еженедельной оценке в ходе терапии.
Как видно из графика, во время курса ТМС средние показатели по большинству когнитивных тестов улучшились. При этом, за исключением теста Бентона и теста «Беглость речевых ответов», прирост показателей был статистически значимым (р<0,05). Наибольшее увеличение показателей к окончанию курса терапии отмечалось по тестам «Счет с переключением» — результаты улучшились на 22,3% (р<0,05), «Кодировка» — результаты улучшились на 20,27% (р<0,05). По остальным тестам прирост показателей был менее значимым: по тесту «10 слов» — 5,79% (р<0,05), по тесту Бентона — 8,46%, по тесту «Беглость речевых ответов» — 0,92%.
Следует отметить, что по тестам «Кодировка» и «Счет с переключением» улучшение было статистически значимым уже после первой недели терапии и составило 8,58% (р<0,05) и 6,32% (р<0,05) соответственно. Данные тесты отражают такие аспекты когнитивной сферы, как исполнительские функции и переключаемость внимания. Таким образом, именно эти функции в наибольшей степени отреагировали на ТМС, в то время как в мнестической сфере не отмечалось значимых изменений в ходе терапии. Это отразилось в несущественной динамике показателей тестов как на вербальную память, так и зрительно-моторную координацию.
Сравнительный анализ динамики когнитивных функций в зависимости от клинической эффективности терапии в 1-й группе (АП+ТМС), показал существенно больший прирост показателей по всем тестам у респондеров (20 больных). На представленной ниже диаграмме отражены изменения показателей когнитивных тестов в результате терапии у респондеров и нонреспондеров 1-й группы (АП+ТМС).
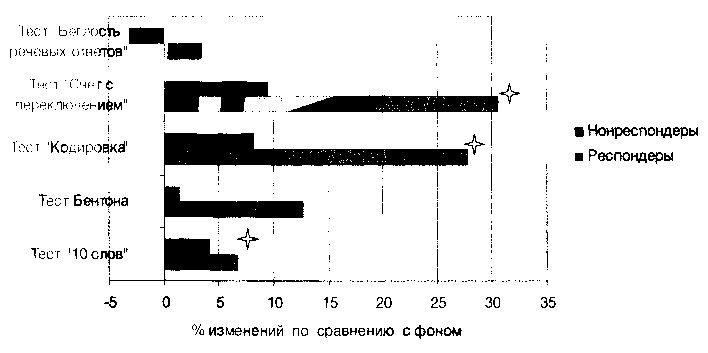
Рис. 3. Изменения показателей когнитивных тестов к окончанию курса ТМС у респондеров и нонреспондеров 1-й группы (АП + ТМС) в процентном отношении
к фоновым значениям
У респондеров статистическая значимость изменений присутствовала в отношении тестов «10 слов», «Кодировка”, «Счет с переключением», с наибольшим улучшением показателей по двум последним: 27,82% (р<0,05) и 30,55% (р<0,05) прироста соответственно. По методике на вербальную память результаты улучшились на 6,73% (р<0,05), а в тесте «Беглость речевых ответов» — лишь на 3,48%. В отношении методики на зрительно-моторную координацию прирост показателей хоть и составил 12,71%, но не был статистически значимым. У нонреспондеров (12 больных) изменения в результатах тестов были невелики и статистически незначимы, более того по тесту «Беглость речевых ответов» отмечалось некоторое ухудшение — уменьшение показателей на 3,2%. По остальным методикам у пациентов с отрицательным ответом на терапию имело место незначительное улучшение результатов: по тесту «10 слов» на 4,16%, по тесту Бентона на 1,35%, по тесту «Кодировка» на 8,16%, по тесту «Счет с переключением» на 9,55%, т.е. существенно меньше, чем у респондеров.
Несмотря на более выраженное улучшение когнитивных функций у респондеров этой группы, значимых корреляций показателей шкалы CDSS в динамике с изменениями показателей когнитивных тестов не прослеживалось. В тоже время обнаружена умеренно выраженная, но статистически значимая корреляция редукции негативной симптоматики по шкале PANSS к окончанию курса ТМС с улучшением результатов по тесту «Кодировка». Коэффициент корреляции Спирмена между общим баллом по негативной подшкале PANSS и показателями теста «Кодировка» к концу 3-й недели терапии составил -0,42 (р<0,05). При корреляционном анализе динамики отдельных негативных симптомов с результатами когнитивных тестов у больных 1-й группы (АП+ТМС), выявлена обратная связь показателей теста «Кодировка» со следующими пунктами PANSS: «Притупленный аффект», «Эмоциональная отгороженность», «Стереотипное мышление». Коэффициенты Спирмена составили -0,46 (р<0,05), -0,37 (р<0,05), -0,45 (р<0,05) соответственно. Между результатами теста «Беглость речевых ответов» и пунктом PANSS «Нарушения абстрактного мышления» к концу 3-й недели терапии, также установлена обратная связь со значением коэффициента Спирмена -0,40 (р<0,05).
Таким образом, у пациентов 1-й группы (АП+ТМС) в процессе терапии отмечалось улучшение в когнитивной сфере, а именно, в отношении исполнительских функций и переключаемости внимания. Положительные изменения когнитивных функций коррелировали с редукцией негативной симптоматики («Притупленный аффект», «Эмоциональная отгороженность», «Стереотипное мышление», «Нарушения абстрактного мышления») и были более выражены у респондеров.
У пациентов контрольной группы (АП+АД) после присоединения антидепрессанта к базисной антипсихотической терапии отмечалось умеренное и постепенное улучшение когнитивных функций. К концу 3-й недели исследования статистическая значимость прироста показателей имела место в отношении всех когнитивных тестов за исключением теста Бентона. По тесту „10 слов» улучшение составило 8,9% (р<0,05), по тесту „Кодировка» — 11,43% (р<0,05), по тесту „Счет с переключением» — 13,96% (р<0,05), по тесту „Беглость речевых ответов» — 10,72% (р<0,05), по тесту Бентона только 2,17%. Учитывая то, что антипсихотическая терапия в этой группе была стабильной, все изменения когнитивных функций у больных этой группы были связаны с действием антидепрессанта, его клиническими и побочными эффектами.
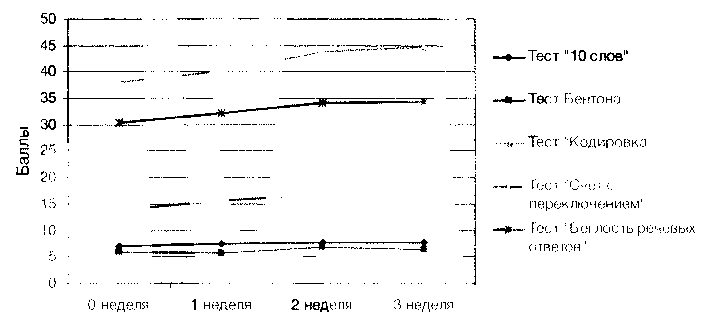
На представленном ниже рисунке 4 показаны результаты когнитивных тестов в контрольной группе (АП+АД) при еженедельной оценке в ходе терапии.
Как и в 1-й группе (АП+ТМС), прирост показателей по тестам на исполнительские функции и переключаемость внимания был наибольшим, однако различия в относительном улучшении результатов с остальными тестами были не столь велики. Обратили на себя внимание достаточно существенные и статистически значимые положительные изменения в тесте на вербальную ассоциативную продукцию, что не было характерным для 1-й группы (АП+ТМС).
В тоже время динамика изменений когнитивных функций в контрольной группе (АП+АД) была не столь стрем тельной, значимое улучшение показателей отмечалось лишь спустя 2 — 3 недели терапии. Это говорит о том, что ТМС оказывает более быстрое стимулирующее влияние на когнитивную сферу, чем гимоаналептическая фармакотерапия.
Сравнительный анализ динамики когнитивных функций у респондеров (18 больных) и нонреспондеров (16 больных) контрольной группы (АП+АД) выявил существенно больший прирост показателей по всем тестам у пациентов, которые положительно ответили на терапию. При этом улучшение по большинству тестов, за исключением теста Бентона, у респондеров было статистически значимым. Наиболее существенно повысились результаты по тестам „Счет с переключением» — 22,76% (р<0,05) и „Беглость речевых ответов» — 18,4% (р<0,05). Стоит заметить, что изначальные показатели по тесту „Беглость речевых ответов» у респондеров были ниже, и даже после их значимого улучшения в процессе терапии лишь приблизились к таковым у нонресподеров. Прирост результатов по тесту „Кодировка» у респондеров контрольной группы (АП+АД) составил 14,71% (р<0,05), что значительно ниже соответствующего показателя у респондеров 1-й группы (АП+ТМС). Это говорит о том, что ТМС в большей степени улучшает исполнительские функции у больных шизофренией, чем тимоаналептическая фармакотерапия.
В отношении мнестических функций прослеживалась обратная тенденция, в контрольной группе (АП+АД) улучшение показателей по тесту „10 слов» у респондеров составило 11,71% (р<0,05), что выше аналогичного значения у респондеров 1-й группы (АП+ТМС). Возможно, фармакотерапия антидепрессантами лучше влияет на вербальную память, чем ТМС. В методике на зрительно-моторную координацию у пациентов с положительным ответом на терапию улучшение составило 10,42%, но не было статистически значимым. У пациентов контрольной группы (АП+АД), негативно ответивших на терапию, изменения в когнитивной сфере были минимальны и статистически незначимы. Более того, по тесту Бентона отмечалось некоторое ухудшение — снижение показателей на 6,37%. По остальным методикам у нонреспондеров имело место незначительное улучшение результатов: по тесту „10 слов» на 5,83%, по тесту „Кодировка» на 7,4%, по тесту „Счет с переключеием“ на 4,45%, по тесту „Беглость речевых ответов» на 3,36%. На представленном ниже рисунке 5 отражены изменения показателей когнитивных тестов в результате терапии у респондеров и нонреспондеров контрольной группы (АП+АД).

Рис. 5. Изменения показателей когнитивных тестов к концу 3-й недели терапии у респондеров и нонреспондеров контрольной группы (АП+АД) в процентном отношении к фоновым значениям + р<0,05
Несмотря на более существенное улучшение когнитивных функций у больных, которые положительно ответили на терапию, значимых корреляций в динамике психометрических показателей и результатов когнитивных тестов в контрольной группе выявлено не было. В тоже время корреляционной анализ, проведенный отдельно у респондеров и нонреспондеров этой группы выявил статистически значимые корреляции показателей шкалы CDSS и результатов теста Бентона к концу 3-й недели терапии. У респондеров корреляция была отрицательной, коэффициент корреляции Спирмена составил -0,60 (р<0,05), у нонреспондеров — положительной со значением коэффициента 0,61 (р<0,05). То есть, в случае положительного ответа на терапию, показатели зрительно-моторной координации улучшались по мере редукции депрессивной симптоматики.
Таким образом, для контрольной группы (АП+АД) было характерно более постепенное и менее выраженное улучшение в когнитивной сфере по сравнению с 1-й группой (АП+ТМС). У респондеров прирост когнитивных показателей был больше, мри :>том результаты теста Бентона коррелировали с редукцией депрессии. В сравнении с 1-й группой (АП+ТМС) улучшение исполнительских функций в контрольной группе (АП+АД) не столь отчетливо преобладало над положительными изменениями в других сферах, в частности мнестической.
В группе резистентных больных при подключении к психофармакотерапии ТМС отмечалось улучшение по всем когнитивным тестам. При этом динамика прироста когнитивных показателей была более выражена, чем в контрольной группе (АП+АД). К концу 3-й недели терапии статистически значимое улучшение отмечалось по всем тестам за исключением теста Бентона. Также как и в 1-й группе (АП+ТМС), у резистентных больных в наибольшей степени улучшились результаты тестов на исполнительские функции и переключаемость внимания. Прирост показателей к окончанию курса ТМС по тесту „Счет с переключением» составил 23,53% (р<0,05), по тесту „Кодировка» — 17,4% (р<0,05). Следует отметить, что уже к концу 1-й недели терапии улучшение по этим тестам имело статистическую значимость и составило 11,8% (р<0,05) по тесту „Счет с переключением» и 5,44% (р<0,05) по тесту „Кодировка».
Прирост показателей по тесту „Счет с переключением» в группе резистентных больных (АП+АД+ТМС) был более выражен, чем в двух других группах на всех этапах лечения. При этом различия в динамике по этому тесту с контрольной группой (АП+АД) были более существенными, чем с 1-й группой (АП+ТМС). По тестам на вербальную память, зрительно-моторную координацию и вербальную ассоциативную продукцию улучшение в 3-й группе (АП+АД+ТМС) было не таким выраженным, как по тестам на исполнительские функции и пере-ключаемость внимания. К концу курса ТМС прирост показателей по тесту „10 слов» составил 8,96% (р<0,05), по тесту Бентона — 8,54%, по тесту „Беглость речевых ответов» — 12,62% (р<0,05). В начале лечения изменения по этим тестам были несущественными и статистически незначимыми.
На представленном ниже рисунке 6 показаны результаты когнитивных тестов в 3-й группе (АП+АД+ТМС) при еженедельной оценке в ходе терапии.
Анализ динамики когнитивных функций у респондеров (20 больных) и нонреспондеров (11 больных) в группе терапевтически резистентных больных (АП+АД+ТМС) выявил более существенное улучшение по большинству методик у пациентов, положительно ответивших на терапию. У респондеров отмечался статистически значимый прирост показателей по всем тестам, за исключением теста Бентона, у нонреспондеров — только по тестам „Кодировка» и „Счет с переключением».
У больных с положительным ответом на терапию улучшение по тесту „10 слов» к окончанию курса ТМС составило 8,16% (р<0,05), по тесту Бентона — 10,3%, по тесту „Кодировка» -20,99% (р<0,05), по тесту „Счет с переключением» — 26,33% (р<0,05), по тесту „Беглость речевых ответов» — 17,15%. Стоит отметить, что прирост показателей по тесту „Счет с переключением» у респондеров был статистически значимым уже после первой недели терапии и составил 13,62% (р<0,05). У пациентов, отрицательно ответивших на лечение, показатели по тесту „10 слов» увеличились на 10,78% (р<0,05), по тесту Бентона — на 5,9%, по тесту „Кодировка» -на 11,42% (р<0,05), по тесту „Счет с переключением» — на 19,35%, по тесту „Беглость речевых ответов» — на 5,1%. Только в методике на вербальную память нонреспондеры несколько превзошли в улучшении респондеров, по остальным тестам ситуация была обратной. Наиболее существенно динамика прироста показателей различалась в методиках на исполнительские функции и вербальную ассоциативную продукцию. На представленном ниже рисунке 7 отражены изменения показателей когнитивных тестов в результате терапии у респондеров и нонреспондеров группы резистентных больных (АП+АД+ТМС).
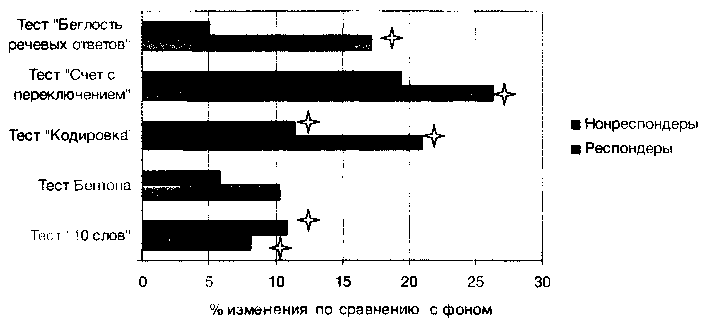
Рис. 7. Изменения показателей когнитивных тестов к окончанию курса ТМС у респондеров и нонреспондеров 3-й группы (АП + АД + ТМС) в процентном отношении к фоновым значениям — р<0,05
Несмотря на более чем трехкратные различия в относительном приросте показателей по методике «Беглость речевых ответов» (респондеры — 17,15%, нонреспондеры — 5,1%), изначальные показатели по этому тесту у больных с положительным ответом на терапию были ниже на 8,48%. Т. е. для респондеров была характерна более выраженная идеаторная заторможенность, которая уходила во время курса ТМС. Помимо этого, у нонреспондеров показатели по шкале CDSS на момент включения в исследование положительно коррелировали с результатами теста «Беглость речевых ответов». Коэффициент корреляции Спирмена составлял 0,66 (р<0,05). Т. е. больные с более выраженной депрессией давали большее число речевых ответов в этом тесте. Это свидетельствует о том, что отсутствие идеаторной заторможенности и соответственно более высокие результаты по методике на вербальную ассоциативную продукцию при резистентных депрессиях у больных шизофренией связано с менее вероятным положительным ответом на лечение ТМС.
Корреляционный анализ не выявил значимой связи динамики депрессивной симптоматики и общего балла по негативной подшкале PANSS ни с одним из когнитивных тестов. В то же время в группе резистентных больных (АП+АД+ТМС) к окончанию курса ТМС отмечались значимые отрицательные корреляции всех когнитивных тестов с такими пунктами PANSS, как «Нарушения абстрактного мышления» и «Стереотипное мышление». В наибольшей степени «Нарушения абстрактного мышления» коррелировали с результатами теста «Беглость речевых ответов». При этом коэффициент Спирмена составил -0,71 (р<0,05), что говорит о достаточно тесной обратной связи. Стоит отметить, что показатели теста «Беглость речевых ответов» к концу курса терапии в значимой мере отрицательно коррелировали со всеми пунктами негативной подшкалы PANSS, за исключением пункта «Пассивно-апатическая социальная отгороженность». У респондеров прослеживались отрицательные корреляции выраженности негативной симптоматики с результатами методик на исполнительские функции, переключаемость внимания и вербальную ассоциативную продукцию, как до терапии, так и во время нее.
Коэффициент корреляции Спирмена между показателями негативной подшкалы PANSS и теста «Кодировка» к окончанию курса ТМС составил -0,48 (р<0,05). Для тестов «Счет с переключением» и «Беглость речевых ответов» эти коэффициенты составили -0,50 (р<0,05) и -0,62 (р<0,05) соответственно. Также как у группы в целом, у респондеров прослеживались отрицательные корреляции практически всех когнитивных тестов с такими пунктами PANSS, как «Нарушения абстрактного мышления» и «Стереотипное мышление». С наибольшим числом негативных симптомов у респондеров коррелировали показатели теста «Беглость речевых ответов». Результаты теста «Счет с переключением» к концу курса ТМС у больных с положительным ответом на терапию отрицательно коррелировали с пунктом PANSS «Пассивно-апатическая социальная отгороженность», коэффициент Спирмена составил -0,56 (р<0,05).
Таким образом, в процессе лечения ТМС у резистентных больных отмечалось улучшение когнитивного функционирования, преимущественно по методикам, отражающим исполнительские функции и переключаемость внимания. Прирост показателей по большинству тестов был достаточно быстрым, коррелировал с редукцией негативной симптоматики и преобладал у респондерон.
Обсуждение и выводы
Результаты данного исследования свидетельствуют о том, что циклическая ТМС по своим тимоаналептическим свойствам не уступает традиционным методам терапии этих состояний. К преимуществам этого метода можно отнести быстроту развития анидепрессивного эффекта по сравнению с психофармакотерапией, а также достаточно высокую эффективность при резистентных депрессиях в рамках шизофрении. Помимо этого для ТМС было характерно более выраженное действие на негативную симптоматику, вероятнее всего на вторичную, ассоциированную с депрессией. Стоит обратить внимание на изначально более низкие показатели по большинству когнитивных тестов у больных шизофренией, в сравнении с таковыми у пациентов с резистентными депрессиями. Улучшение когнитивных функций в процессе терапии отмечалось во всех группах и преобладало у респондеров, что косвенно свидетельствует о связи положительных изменений в когнитивной сфере с редукцией депрессии. Однако в большей мере связь когнитивных нарушений прослеживалась с выраженностью негативной симптоматики, при этом по мере редукции последней в процессе терапии ТМС когнитивные функции улучшались.
В наибольшей степени у больных шизофренией с депрессивной симптоматикой во время лечения возросли показатели тестов на исполнительские функции и переключаемость внимания. Стоит отметить, что в группах, где проводилась ТМС, эти функции улучшались быстрее и в большей степени, особенно у респондеров. По всей видимости, это связано с тем, что нарушение исполнительских функций и переключаемости внимания связано с дисфункцией префронтальной коры, на которую и оказывалось стимулирующее воздействие. Исходя из этого, значимое улучшение по тестам „Кодировка» и „Счет с переключением» в начале курса ТМС может рассматриваться как прогностически благоприятный фактор положительного ответа на терапию. В тоже время отсутствие идеаторной заторможенности и соответственно более высокие показатели по тесту „Беглость речевых ответов» связаны с неэффективностью ТМС в группе резистентных больных.
Аналогичная, но менее выраженная взаимосвязь вербальной ассоциативной продуктивности до начала лечения с эффективностью терапии прослеживалась и в других группах. Исследование вербальной памяти выявило более выраженное улучшение по тесту «10 слов» у респондеров контрольной группы, что, по всей видимости, связано с положительным эффектом тимоаналептической фармакотерапии на мнестические функции. Положительные изменения в когнитивной сфере, достигнутые в процессе терапии, были достаточно стойкими, лишь у отдельных больных по завершении курса ТМС отмечалась обратная динамика когнитивных показателей. Возможно это связано с исчерпыванием стимулирующего действия ТМС на когнитивные функции у некоторых больных. Другой вероятной причиной ухудшения показателей когнитивных тестов после прекращения ТМС являлся частичный возврат депрессивной симптоматики у некоторых больных. Недостатком данного исследования является отсутствие плацебо-контроля, что снижает научную достоверность результатов. Однако проведение псевдо-ТМС в значительной мере усложнило бы исследование с технической стороны, а также имеет этические ограничения.
Результаты нашего исследования в целом согласуются с данными Пуговкиной О.Д. (Пуговкина О.Д. с соавт., 2006), выявившей стимулирующее действие ТМС на когнитивные функции у больных с терапевтически резистентными депрессиями. Отличием являлось то, что у пациентов с шизофренией не наблюдалось значимого улучшения показателей зрительно-моторной координации при лечении этим методом. Данные многих международных исследований также свидетельствуют в пользу положительного влияния высокочастотной ТМС левой дорсолатеральной префронтальной коры на когнитивные функции, а именно на беглость речи, когнитивную гибкость, рабочую и вербальную память (Guse В. et al., 2010). При этом в исследованиях, в которых использовались более высокие частоты стимуляции, были получены лучшие результаты. Применение нейронавигации с помощью функциональной магнитно-резонансной томографии существенно повышало эффективность терапии, как в клиническом, так и в нейропсихологическом аспектах (Sack А. Т. et al., 2003, 2009). Работы в основном проводились у больных депрессиями, данные в отношении влияния ТМС на когнитивные функции у больных шизофренией ограничены (Mittrach М. et al., 2010).
Таким образом, наше исследование показало, что циклическая ТМС по своим тимоаналептическим свойствам не уступает традиционным методам психофармакотерапии депрессий в рамках шизофрении, обладает противорезистентным действием, а также улучшает когнитивные функции. Несмотря на предварительные обнадеживающие результаты, применение этой методики, особенно у больных шизофренией, остается малоизученным и требует проведения дополнительных исследований.
Литература:
- Martin R. L., Cloninger С. R., Guze S. В., Clayton RJ. Frequency and differential diagnosis of depressive syndromes in schizophrenia//J. Clin. Psychiatry, 1985, N° 46, p. 9-13.
- Birchwood M., Mason R., Macmillan E, Healy J. Depression, demoralization and control over psychotic illness* a comparison of depressed and non-depressed patients with a chronic psychosis// Psychol. Med, 1993, № 23, p. 387-395.
- Johnson D. A. W.: The significance of depression in the prediction of relapse in chronic schizophrenia//Br.J. Psychiatry, 1988, № 15, p. 2320-2323.
- Mandel M. R., Severe J. B., Schooler N. R., Gelenberg A.J., Mieske M. Development and prediction of postpsychotic depression in neuroleptic-treated schizophrenics//Arch. Gen. Psychiatry 1982, № 39, p. 197-203.
- Roy A., Thompson R., Kennedy S. Depression in chronic schizophrenia//Br.J. Psychiatry, 1983, № 142, p. 465-470.
- Norholm V., Bech P. Quality of life in schizophrenic patients: association with depressive symptoms//Nord J. Psychiatry, 2006, N° 60 (1), p. 32-37.
- Мосолов C.H. Клиническое применение современных антидепрессантов. СПб.: Медицинское информационное агентство, 1995, с. 209-352.
- Wolf С. Brain activity supporting working memory accuracy in patients with paranoid schizophrenia: a functional magnetic resonance imaging study//Neuropsychobiology, 2011, № 64 (2), p. 93-101
- Molina V. Association between cerebral metabolic and structural abnormalities and cognitive performance in schizophrenia//Psychyatry Res., 2009, № 173 (2), p. 88-93.
- Ettinger U. Functional magnetic resonance imaging of a parametric working memory task in schizophrenia: relationship with performance and effects of antipsychotic treatment// Psychopharmacology (Berl)., 2011, N° 216 (1), p. 17-27
- Holtzheimer P. E., Russo J., Avery D. H. A meta-analysis of repetitive transcranial magnetic stimulation in the treatment of depression//Psychopharmacol. Bull., 2001, N° 35 (4), p. 149-169.
- Пуговкина О. Д. Когнитивное функционирование и его динамика у больных терапевтически резистентными депрессиями в процессе лечения методами электросудорожной терапии и транскраниальной магнитной стимуляции: Диссертация на соискание ученой степени кандидата психологических наук. М., 2006.
- Пуговкина О. Д., Холмогорова А. Б., Цукарзи Э. Э., Ильин С. А., Мосолов С. Н. Динамика когнитивных функций у пациентов с резистентными депрессиями при применении электросудорожной терапии (ЭСТ) и циклической транскраниальной магнитной стимуляцией (цТМС)//Социальная и клиническая психиатрия, 2006, № 2, с. 47-51.
- Иванов М.В., Незнанов Н.Г. Негативные и когнитивные расстройства при эндогенных психозах: диагностика, клиника, терапия. Спб.: Изд. НИПНИ им. В. М. Бехтерева, 2008, с. 36-40.
- Addington D., Addington J., Maticka-Tyndale E. Reliability and validity of depression rating scale for schizophrenics. A structured interview guide for the Hamilton Depression Rating Scale// Schizophrenia Res., 1992, Vol. 6, p. 201-208.
- Guse B., Falkai P., Wobrock T. Cognitive effects of high-frequency repetitive transcranial magnetic stimulation: a systematic review//J Neural Transm., 2010, Vol. 117, № 1, p. 105-122.
- Sack A.T., Linden D. E. Combining transcranial magnetic stimulation and functional imaging in cognitive brain research: possibilities and limitations//Brain Res. Rev., 2003, Vol. 43, № 1, p. 41-56.
- Sack A.T. Optimizing functional accuracy of TMS in cognitive studies: a comparison of methods. J. Cogn Neurosci, 2009, Vol. 21, № 2, p. 207-221.
- Mittrach M. et al. The tolerability of rTMS treatment in schizophrenia with respect to cognitive function//Pharmacopsychiatry, 2010, Vol. 43, № 3, p. 110-117.
ДЛЯ ЗАМЕТОК
- Издание подготовлено рекламным агентством ООО «Проссима;
Компьютерная верстка Андрей Ларионов. - У больных аффективными расстройствами и их родственников были обнаружены специальные генные локусы, ответственные за недостаточность функции биологических часов в организме и повышающие риск развития депрессии (Kupfer D.J., Frank Е., 2005).
- Исключение составляет кломипрамин, доза которого при поддерживающей терапии может быть значительно ниже лечебной (Pato М.Т. с соавт., 1990).