Целью исследования являлась оценка клинической эффективности комбинированной терапии оланзапин-ЭСТ и клозапин-ЭСТ в случаях резистентной шизофрении, а также выявление прогностических факторов, влияющих на эффективность присоединения ЭСТ к клозапину и олапзапину. Анализ полученных результатов позволил сделать вывод об эффективности всех рассматриваемых способов преодоления резистентности, при этом группы оланзапина и клозапина в целом были сопоставимы между собой, также как и соответствующие группы комбинированной терапии. Было установлено, что в группах комбинированной терапии эффект достигался в более короткие сроки и был более глубоким, при сопоставимом количестве респондеров. Результаты корреляционного и множественного регрессионного анализа показали, что предиктивное значение для достижения эффекта в группах комбинированной терапии имеет депрессивная, негативная и кататоническая симптоматика.
Современные алгоритмы фармакотерапии резистентных психозов, разрабатываемые на основании систематизированных анализов контролируемых исследований и консенсусных решений, предлагают две терапевтические стратегии.
В первую очередь, это лечение антипсихотиками с ожидаемым воздействием на резистентность. Другой стратегией является усиление эффекта антипсихотической терапии (использование комбинаций нейролептиков, назначение высоких дозировок, метод «зигзага» и т.д.), либо применение так называемой «аугментации» или «наслаивания» (комбинирование нейролептиков с препаратами других групп).
Еще одним терапевтическим направлением при резистентной шизофрении является применение нелекарственных методов, имеющих особые традиции в отечественной психиатрии.
Нелекарственные методы включают «шоковые методы» и специальные методики, способные изменять реактивность организма и усиливать терапевтический ответ (гемосорбция, плазмаферез).
Так называемые «шоковые методы» (инсулинокоматозная и электросудорожная терапия) имеют более давнюю историю применения при резистентной шизофрении. Изначально, теоретическим обоснованием применения ЭСТ при шизофрении была известная концепция об антагонистическом влиянии эпилептических припадков на психотическую симптоматику и в целом на прогредиентность течения шизофрении. Однако, оказалось, что эффективность ЭСТ как монотерапии при резистентной шизофрении невысока — эффект достигался у 5-10% резистентных больных (Morrison D., 1996). В настоящее время ЭСТ не рассматривается как метод, применяемый при лечении резистентной шизофрении. В качестве отдельных показаний к применению ЭСТ при шизофрении являются тяжелая депрессия и кататоническая симптоматика.
«Золотым стандартом» противорезистентного антипсихотика является клозапин. По данным разных авторов, клозапин эффективен примерно у трети резистентных больных шизофренией (Kane J. et al, 1988; Breier А., 1993; Marder S. et al., 1995; Conley R., 1998).Однако очевидны определенные ограничения применения клозапина в высоких дозах и длительными курсами, в первую очередь из-за риска возникновения агранулоцитоза и гранулоцитопении, метаболических нарушений, а также появления спонтанной судорожной активности и изменений на ЭКГ.
Сходство химической структуры, а также близкий спектр нейрохимической активности клозапина и оланзапина позволяют предположить их сходные терапевтические возможности в качестве антипсихотиков с противорезистентной активностью. К настоящему времени противорезистентная активность оланзапина, применяемого в виде монотерапии, показана во многих исследованиях (Chouinard G. et al., 1993; Smith R. et al., 1996; Breier A., 1999; Volavka J. et al., 2004 и др.).
Недостаточная эффективность психофармакотерапии при резистентной шизофрении является обоснованием применения методов нелекарственной терапии, способных изменять реактивность организма и усиливать терапевтический ответ (гемосорбция, плазмаферез, внутривенное лазерное облучение крови). Однако отсутствие доказательных, контролируемых исследований по клиническому применению этих методов приводит к противоречивости оценок их эффективности.
В течение длительного времени в литературе обсуждается возможность комбинированного применения в случаях резистентной шизофрении ЭСТ и клозапина (Fink М., 1990; Meltzer H.Y., 1990). Кроме того, рассматриваются перспективы применения ЭСТ при так называемой «ультрарезистентной» шизофрении или шизофрении, резистентной к лечению клозапином. В этих случаях предполагается присоединение ЭСТ к неэффективной терапии клозапином в качестве метода аугментации. Однако главным недостатком упомянутых выше работ являлось использование малых групп пациентов, либо имело место описание отдельных клинических наблюдений. Целью настоящего исследования являлась оценка клинической эффективности и переносимости комбинированной терапии оланзапином и ЭСТ и клозапином и ЭСТ у больных шизофренией, резистентной к адекватной антипсихотической терапии.
Материал и методы исследования
В исследование включались больные шизофренией, резистентные к адекватной антипсихотической фармакотерапии, находившиеся на лечении в отделениях психиатрической больницы № 4, а также отделении интенсивной терапии МНИИП Росздрава. Под резистентностью подразумевалось отсутствие терапевтического ответа на последовательно проводившееся лечение как минимум двумя нейролептиками различных химических классов. При этом суточные дозы препаратов должны были быть адекватны 700 мг/сут аминазинового эквивалента, а продолжительность курса терапии составлять не менее 6 недель каждым препаратом.
После проведения скрининга и получения информированного согласия пациенты рандомизированно распределялись в 4 терапевтические группы: монотерапии оланзапином или клозапином и комбинированной клозапином с ЭСТ и оланзапином с ЭСТ. В течение первых 7 дней проводилась замена прежнего лечения на исследуемый препарат. Продолжительность периода активной терапии составила 10 недель. Оланзапин и клозапин назначались в адекватных терапевтических дозах с учетом индивидуальной переносимости: оланзапин — в диапазоне 10-20 мг, клозапин — 200-900 мг в сутки. Суточные дозы исследуемых препаратов в группах комбинированной терапии во время всего курса оставались неизменными. В группах комбинированной терапии пациентам проводился курс из 8-18 сеансов ЭСТ с билатеральным наложением электродов (2 сеанса в неделю). Процедуры ЭСТ проводились на аппарате ЭЛ И КОН-01 под общей анестезией.
Оценка выраженности симптоматики проводилась на скрининге, в конце 1-й, 2-й, 4-й, 6-й, 8-й и 10-й недели терапии по шкалам PANSS, CGI и MOSES (Monitoring Of Side Effects Scale, Kalachnik J. E. 1988). Основным критерием эффективности являлась редукция симптоматики по шкале PANSS более 20% от исходного уровня.
В окончательный анализ настоящего исследования вошли данные по 80 больным, из них 21 пациент входил в группу клозапина, 21 пациент — в группу оланзапина, 19 пациентов — в группу клозапин + ЭСТ, 19 — в группу оланзапин + ЭСТ.
Диагноз шизофрении был выставлен в соответствии с критериями МКБ-10. В целом, группы были сопоставимы по клинико-демографическим характеристикам.
Обработка полученных данных проводилась в соответствии с общепринятыми в медицине методами одномерной и многомерной статистики. Расчет количественных показателей с нормальным распределением проводился по стандартному t-критерию Стьюдента, расчет качественных показателей — по критерию х2 с последующим определением коэффициента сопряженности. С целью повышения статистической мощности исследования и выявления симптоматики, наиболее чувствительной к присоединению к терапии атипичным антипсихотиком ЭСТ, были проведены корреляционный и регрессионный анализы объединенной группы монотерапии и объединенной группы комбинированной терапии. В регрессионном анализе была использована модель пошаговой обратной множественной регрессии (Backward stepwise). В качестве зависимого признака (переменной отклика) было взято наличие или отсутствие терапевтического эффекта у пациента, выражаемое в редукции симптоматики по PANSS более 20%.
В качестве независимых переменных были выбраны признаки, достоверно коррелирующие с достижением эффекта в корреляционной матрице, а также симптомы, в отношении которых предполагается эффективность терапии. С целью проверки возможности применения полученного уравнения при прогнозировании эффективности терапии при резистентной шизофрении, были набраны две проверочные группы, в каждую из которых вошли 10 резистентных к фармакотерапии больных шизофренией, удовлетворяющих критериям включения в исследование и не имеющих значимых клинико-демографических различий с основной группой монотерапии. У всех пациентов дважды было проведено шкалирование по PANSS: до начала лечения и после 10 недель терапии. В группе монотерапии пациенты получали клозапин или оланзапин в адекватных терапевтических дозировках, в группе комбинированной терапии дополнительно проводились процедуры ЭСТ. В случае если редукция симптоматики превышала 20% от исходной, пациент считался респондером, если нет — нонреспондером. Затем, подставляя цифровые значения, соответствующие исходной выраженности каждого из симптомов уравнения, мы умножали их на приведенные в уравнении коэффициенты, соответствующие каждому симптому. Таким образом, было получено цифровое значение, которое характеризует прогнозируемую эффективность. Следующим шагом стало проведение корреляционного анализа между прогнозируемым и фактическим результатом.
Обработка данных происходила с использованием программ BIOSTAT («программа БИОСТАТИСТИКА для WINDOWS и DOS IBM-PC») и Statistica 6.0.
Результаты
Анализ полученных результатов позволил сделать вывод об эффективности всех рассматриваемых способов преодоления резистентности, при этом группы оланзапина и клозапина в целом были сопоставимы между собой, также как и соответствующие группы комбинированной терапии. При сравнении групп монотерапии с группами комбинированной терапии были получены следующие данные. По количеству респондеров преимуществ в группах комбинированной терапии не отмечалось, тогда как глубина эффекта (то есть степень редукции симптоматики) была достоверно выше в группах комбинированной терапии. Кроме того, группы комбинированной терапии превосходили группы монотерапии по скорости наступления эффекта (Оленева Е. В., Цукарзи Э.Э, Мосолов С. Н. 2007).
Построение корреляционной матрицы объединенной группы монотерапии выявило следующие интересные закономерности. Выявлена положительная достоверная взаимосвязь эффекта (редукции симптоматики по PANSS более 20%) и единственного признака -возбуждение. Тогда как отрицательная достоверная корреляция выявлена при оценке взаимосвязи таких признаков, как притупление аффекта и депрессия (табл. 1). Наличие положительной корреляции с возбуждением, по всей видимости, объясняется наличием выраженного седативного действия у обоих препаратов группы. Такой пункт шкалы PANSS как возбуждение, являясь показателем остроты состояния, клинически тесно ассоциирован с кататоно-гебефренной симптоматикой, большая часть которой подвергается редукции под действием именно антипсихотиков с седативным действием.

Таблица 1. Коэффициенты корреляции значимых признаков с эффективностью монотерапии атипичными антипсихотиками (редукция по PANSS>20%)
Наличие взаимосвязи с такими симптомами, как депрессия и притупление аффекта, вновь возвращает нас к вопросу о дифференциации негативной и депрессивной симптоматики. К сожалению, шкала PANSS не дает возможности достоверно разграничить столь близкую по своим проявлениям симптоматику. Требуемый при заполнении PANSS формальный подход к оцениваемому симптому, невозможность трактовать то, что видишь, приводит к необходимости при наличии депрессивной симптоматики высоко оценивать такие пункты негативной подшкалы PANSS, как «притупленный аффект», «эмоциональная отстраненность», «трудности в общении», нередко — «пассивно-апатическая социальная отгороженность». То есть, по сути, при оценке по PANSS возможно изолированное существование негативной симптоматики без симптомов депрессии, но невозможно наличие депрессии без негативной симптоматики.
Таким образом, получение отрицательной корреляции между достижением эффекта, депрессией и притуплением аффекта, по всей видимости, связано с отсутствием у рассматриваемых антипсихотиков антидепрессивного действия. Судить о наличии или отсутствии влияния на негативную симптоматику не представляется возможным.
Для более точной оценки параметров, влияющих на возможность ответа на терапию атипичным антипсихотиком, был проведен регрессионный анализ. Всего в анализ было включено 42 пациента, получавших терапию клозапином и оланзапином.
В качестве независимых переменных были выбраны признаки, достоверно коррелирующие с достижением эффекта в корреляционной матрице — возбуждение, депрессия и притупление аффекта, а также симптомы, в отношении которых предполагается эффективность комбинированной терапии, для дальнейшего сравнения -манерность, заторможенность, эмоциональная отгороженность.
Таким образом, при обратной пошаговой множественной регрессии были получены следующие значимые переменные: депрессия, притупление аффекта, возбуждение (табл. 2).
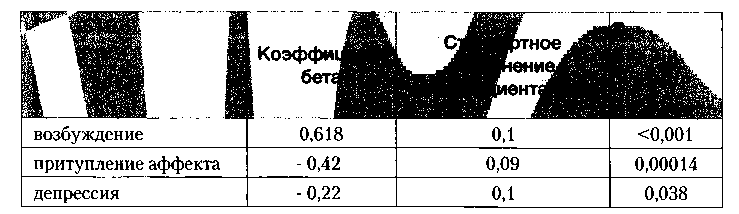
Таблица 2. Характеристика предиктивных признаков эффективности монотерапии атипичными антипсихотиками при терапевтически резистентной шизофрении
Уравнение множественной регрессии в этом случае выглядит следующим образом:
- Y= 0,618х (возбуждение) — 0,42х (притупление аффекта) — 0,22 х (депрессия).
В целом данная модель показала предиктивные значения признаков в 79% случаев, и объяснило 59% наблюдаемой дисперсии. Остальные переменные не достигли уровня статистической значимости для прогноза.
Значение F критерия для модели в целом было равно 11,02, статистическая значимость р < 0,001.
Результаты проверки полученных регрессионных уравнений на проверочной группе показали их высокую сопоставимость, корреляция между прогнозируемым и фактическим значением составила 0,77 (р<0,001) (рис. 1).
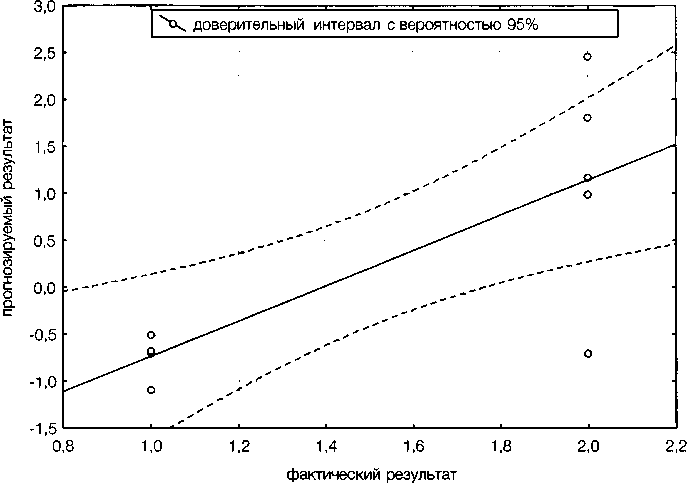
Рис. 1. Сопоставление фактической и прогнозируемой оценок эффективности монотерапии атипичными антипсихотиками при терапевтически резистентной шизофрении
прогнозируемый результат = -2,614 + 1,8792 * фактический результат Корреляция: г = 0,77776
Таким образом, вероятность достижения эффекта при использовании монотерапии клозапином или оланзапином больше у пациентов с наличием возбуждения и без признаков депрессии.
Построение корреляционной матрицы объединенной группы комбинированной терапии выявило следующие закономерности. Значимые положительные корреляции с достижением эффекта были достигнуты по следующим признакам, представленным пунктами шкалы PANSS: возбуждение, притупление аффекта, эмоциональная отгороженность, трудности в общении, манерность, депрессия, заторможенность (табл. 3).

Таблица 3. Коэффициенты корреляции значимых признаков с эффективностью комбинированной терапии (редукция по PANSS>20%)
Таким образом, эффект взаимосвязан с фоновыми проявлениями возбуждения, кататонии (манерность), депрессии или негативной симптоматики (притупление аффекта, эмоциональная отгороженность, трудности в общении). Необходимо отметить, что перечисленные симптомы достаточно трудно достоверно оценить в изолированном, вырванном из контекста конкретной клинической ситуации случае. Так, симптом заторможенность в рамках данной корреляционной матрицы достоверно взаимосвязан как с вышеупомянутыми проявлениями негативной симптоматики, так и с депрессией или с кататонией. Это вполне очевидно клинически, поскольку моторная заторможенность может наблюдаться и в рамках кататонического синдрома, и при депрессии, а учитывая формализованность оценки пунктов PANSS, может характеризовать и поведение больного с выраженной негативной симптоматикой. То же самое можно отнести и к возбуждению, которое может быть не только проявлением продуктивных расстройств, в подшкалу которых входит, но и кататонических нарушений, и ажитации при депрессии. Симптомы, относящиеся к негативной подшкале, при наличии у пациента депрессии могут характеризовать депрессивный статус, а не дефицитарные расстройства. Последнее наблюдение вновь возвращает нас к вопросу о недостатках шкалы PANSS и невозможности в рамках данного исследования выявления влияния комбинированной терапии на первичную негативную симптоматику.
Таким образом, можно выделить четыре условных группы клинических признаков, связанных с достижением эффекта при использовании комбинированной терапии — кататонические расстройства, депрессия и тесно переплетенные с ней негативные нарушения, и симптомы возбуждения.
Для уточнения параметров, влияющих на возможность ответа на комбинированную терапию ЭСТ — атипичный антипсихотик, вновь была использована модель пошаговой обратной множественной регрессии (Backward stepwise). Всего в анализ было включено 38 пациентов, получавших комбинированную терапию клозапин-ЭСТ и оланзапин-ЭСТ.
В качестве независимых переменных были выбраны признаки, рассматриваемые при анализе группы монотерапии, а также «трудности в общении”, показавшие достоверную корреляцию с эффектом.
Таким образом, при обратной пошаговой множественной регрессии были получены следующие значимые переменные: эмоциональная отгороженность, манерность и возбуждение (табл. 4).
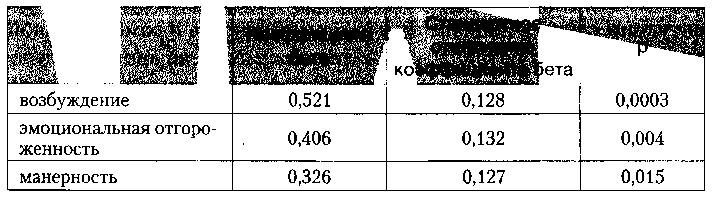
Таблица 4. Характеристика предиктивных признаков комбинированной терапии ЭСТ-атипичный антипсихотик при терапевтически резистентной шизофрении
Уравнение множественной регрессии в этом случае выглядит следующим образом:
- Y= 0,52lx (возбуждение) + 0,406х (эмоциональная отгороженность) + 0,326 х (манерность).
В целом данная модель показала предиктивные значения признаков в 69 % случаев, и объяснило 44 % наблюдаемой дисперсии. Остальные переменные не достигли уровня статистической значимости для прогноза.
Значение F критерия для модели в целом было равно 10,59, статистическая значимость р=0,000046.
Результаты проверки полученных регрессионных уравнений показали их высокую сопоставимость ( коэффициент корреляции между прогнозируемым и фактическим значением — 0,75 (р<0,05)) (рис. 2).
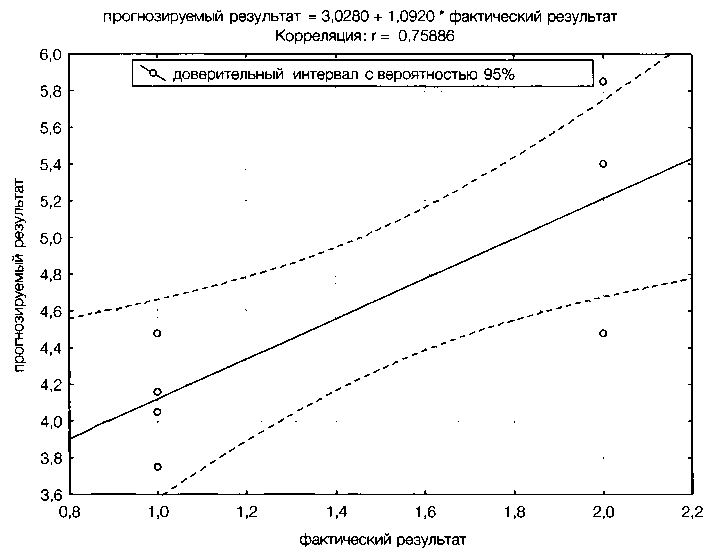
Рис. 2. Сопоставление фактической и прогнозируемой оценок эффективности комбинированной терапии ЭСТ-атипичный антипсихотик при терапевтически резистентной шизофрении
Выполнение данного анализа позволило подтвердить высказанное выше предположение о предиктивном значении наличия кататонической симптоматики, что согласуется с литературными данными. Необходимо отметить, что возбуждение вряд ли можно рассматривать как прогностический фактор эффективности исключительно в группе комбинированной терапии, учитывая, что данный симптом также является предиктором эффективности монотерапии, и, вероятно, в большей мере связан с седативным действием антипсихотика. Выявленная прогностическая важность одного из симптомов негативной подшкалы PANSS, к сожалению, вызывает больше дополнительных вопросов, нежели ответов. Можно ли говорить об избирательной предиктивности именно негативной симптоматики? Учитывая, что в рассмотренной выше корреляционной матрице признак «депрессия» достоверно коррелирует ( r=0,45, р=0,006) с единственным симптомом негативной подшкалы, а именно с «эмоциональной отгороженностью» — вряд ли. Таким образом, в очередной раз камнем преткновения является невозможность в рамках шкалы PANSS четкого разграничения депрессивной и негативной симптоматики, то есть методическая сложность разграничения первичной и вторичной негативной симптоматики.
Переносимость
Говоря о побочных эффектах, необходимо отметить, что большинство из них были связаны с терапией антипсихотиками. У 5 пациентов из групп комбинированной терапии выявлялись жалобы на преходящие нарушения памяти, длительность подобной симптоматики не превышала нескольких дней и не требовала специальной коррекции. Клинически отчетливых когнитивных нарушений также не выявлялось. Следует оговориться, что специальных исследований когнитивных функций не проводилось. И оланзапин, и клозапин вызывали такие побочные эффекты как слабость, седация, головокружение, однако при приеме оланзапина их выраженность была меньше. Кроме того, в пяти случаях возникновения такой побочной симптоматики при приеме оланзапина длительность ее не превышала 1-2 дней и не требовала изменения дозировок. Еще одним общим побочным эффектом являлась прибавка веса. При приеме клозапина этот эффект развивался быстрее, но в целом был менее значительным (к концу исследования у 19 пациентов отмечалась прибавка в весе >5% от исходного, у 7 пациентов >7% от исходного). При приеме оланзапина вес набирался медленнее, но в целом прибавка в весе была более значительной (у 9 пациентов прибавка в весе составила >5% от исходного, у 11 больных >7%), при катамнестическом наблюдении становилось очевидным, что при продолжающемся приеме препарата продолжался и набор веса. Кроме того, в двух случаях побочным эффектом при приеме оланзапина стало возникновение экстрапирамидной симптоматики, для клозапина слюнотечение у 11 пациентов. Гематологических побочных явлений при приеме клозапина не наблюдалось. Значимых изменений ЭКГ, а также показателей АД, пульса и ЧДД отмечено не было, у 4-х пациентов, получавших клозапин, и у 3-х, принимавших оланзапин, отмечалось преходящее снижение АД на первой неделе приема препарата. Повышения судорожной готовности в группах не отмечалось, отставленных судорожных проявлений так же не было.
Обсуждение
Результаты исследования показывают, что наиболее чувствительной к присоединению к монотерапии атипичным антипсихотиком ЭСТ является негативная, депрессивная и кататоническая симптоматика, и, соответственно, фоновая выраженность этих симптомов является предиктором результативности комбинированной терапии. В то же время наличие у пациента депрессии говорит об отрицательном прогнозе монотерапии атипичным антипсихотиком, то есть основные различия между прогностическими признаками достижения эффекта при применении комбинированной и монотерапии лежат в плоскости депрессивной симптоматики. Эффективность ЭСТ при воздействии на депрессивную и кататоническую симптоматику лишний раз подтверждают данные предшествующих исследований (7), тогда как данные о предиктивном значении негативной симптоматики являются в определенной степени новыми. Основной проблемой является невозможность в рамках шкалы PANSS четкого разграничения депрессивной и негативной симптоматики, а также выявление первичной и вторичной негативной симптоматики.
Симптоматика, связанная с возбуждением, является общим предиктором и для комбинированной, и для монотерапии. По всей видимости, эффективность по отношению к этой симптоматике связана с выраженным седативным эффектом обоих рассматриваемых антипсихотиков.
Таким образом, присоединение к терапии атипичным антипсихотиком ЭСТ оправдано при наличии в клинической картине депрессивной, негативной или кататонической симптоматики. Необходимо проведение специальных исследований, направленных на изучение эффективности комбинированной терапии ЭСТ и атипичных антипсихотиков у больных с преобладанием первичной негативной (дефицитарной) симптоматики.
Литература
- Авруцкий Г. Я., Недува А. А. Лечение психически больных. — М: Медицина, 1988.-528 с.
- Зеленина Е. В. Оланзапин у больных шизофренией с признаками терапевтической резистентности//Психиатрия и психофармакотерапия, 2002, том 4, № 4, с. 145-147.
- Мосолов С.Н. Основы психофармакотерапии. — Москва: «Восток», 1996, с. 288.
- Мосолов С.Н. Резистентность к психофармакотерапии и методы ее преодоления// Психиатрия и психофармакотерапия, 2002, том 4, № 4, с. 132-136.
- Наливкина Е. А. Преодоление терапевтической резистентности атипичными антипсихо-тиками у больных параноидной шизофренией//Новые достижения в терапии психических заболеваний/Под ред. профессора Мосолова С. Н. — М.: ЗАО «Издательство БИНОМ», 2002, с. 201-208
- Оленева Е. В., Цукарзи Э.Э, Мосолов С. Н. Комбинированное применение ЭСТ и атипичных антипсихотиков у больных шизофренией, резистентных к терапии//Социальная и клиническая психиатрия, 2007, выпуск 4, с. 28-33.
- Серейский М.Я. Судорожная терапия шизофрении//Невроп. и психиат., 1938, том 7, № 12, с. 3-25.
- Benatov R., Sirota Р., Mcgged S. Neuroleptic-resistant schizophrenia treated with clozapine and ECT//ConvulsiveTher., 1996, Vol. 12, p. 117-21.
- Breier A. Clozapine treatment of outpatients with schizophrenia: outcomes and long-term response patterns//Hosp. Community Psychiatry, 1993.- Vol. 44, p. 1145-1149.
- Breier A, Hamilton S. Comparative efficacy of olanzapine and haloperidol for patients with treatment-resistant schizophrenia//Biol Psychiatry, 1999, Vol. 45, p. 403-11
- Conley R., Buchanan R. Evaluation of Treatment-Resistant Schizophrenia//Schizophrenia Bulletin, 1997, Vol. 23 (4), p. 663-674
- Fink M. ECT and clozapine in schizophrenia//} ECT, 1998, Vol. 14, p. 223-226.
- Kane J., Honingfeld G., Singer J. Clozapine for the treatment-resistant schizophrenic: a double-blind comparison with chlorpromazine//Arch. Gen. Psychiatry, 1988, Vol. 45, p. 789-796.
- Kane J. Factors which can make patients difficult to treat//Br.J. Psychiatry, 1996, Vol. 31, p. 10-14.
- Kupchik M., Spivak B. Combined ЕТС-clozapine therapy//J. Clin. Neuropharmacol, 2000, Vol. 23, p. 14-16.
- Morrison D. Management of treatment refractory schizophrenia//British Journal of Psychiatry, 1996, Vol. 169, suppl. 31, p. 15-20.
- Volavka J., Czobor P, Sheitman B. Clozapine, olanzapine, risperidone, and haloperidol in the treatment of patients with chronic schizophrenia and schizoaffective disorder//Am. J. Psychiatry, 2002, Vol. 159, p. 255-262.